
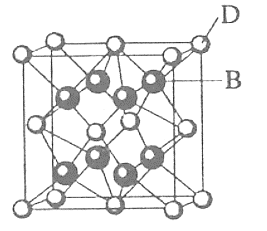
【题目】已知A、B、C、D、E、F都是元素周期表中前36号的元素,它们的原子序数依次增大。A单质是密度最小的气体。B是周期表已知元素中非金属性最强的元素,且和C属同一主族。D、E、F属同一周期,D、F为主族元素,又知E、F的原子序数分别是29、33。D跟B可形成离子化合物,其晶胞结构如图:
(1)比C元素质子数少1的原子的价层电子的轨道表示式为__________。
(2)E元素在周期表中第_____周期,第_____族的元素,它的+2价离子的电子排布式为________。写出E的单质与稀硝酸反应的离子方程式___________。
(3)F元素的名称是_____。与F同一主族的第二、三周期元素与A形成的化合物沸点的高低为___________>__________(用化学式表示),判断的理由____________。
(4)写出D跟A形成的化合物的电子式为________。
【答案】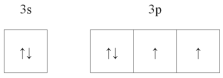 四 ⅠB 1s22s22p63s23p63d9(或[Ar]3d9) 3Cu+8H++2
四 ⅠB 1s22s22p63s23p63d9(或[Ar]3d9) 3Cu+8H++2![]() =3Cu2++NO↑+4H2O 砷 NH3 PH3 NH3可以形成分子间氢键,沸点高
=3Cu2++NO↑+4H2O 砷 NH3 PH3 NH3可以形成分子间氢键,沸点高 ![]()
【解析】
根据题目所给条件,A单质是密度最小的气体,则A为H元素;B是周期表已知元素中非金属性最强的元素,则B为F元素;C与B同主族且A、B、C、D、E、F的原子序数依次增大,则C为Cl元素;E、F的原子序数分别是29、33,则E为Cu元素,F为As元素;D跟B可形成如图所示的晶胞结构,晶胞中D占有8个顶点和6个面心,则晶胞中含有![]() =4个D,8个B全部晶胞内部,则该粒子化合物为DB2,因D为主族元素且原子序数大于Cl小于Cu,则D为Ca元素,据此分析。
=4个D,8个B全部晶胞内部,则该粒子化合物为DB2,因D为主族元素且原子序数大于Cl小于Cu,则D为Ca元素,据此分析。
(1)比Cl元素质子数少1的原子为S原子,其价电子数为6,根据电子排布规则,S原子基态价电子轨道表示式为 ;
;
(2)E为Cu元素,其在元素周期表中的位置为第四周期第ⅠB族,其+2价离子为Cu2+,电子排布式为1s22s22p63s23p63d9(或[Ar]3d9);Cu与稀硝酸反应的离子方程式为3Cu+8H++2![]() =3Cu2++NO↑+4H2O;
=3Cu2++NO↑+4H2O;
(3)F的元素名称为砷,与其同主族的第二、三周期元素为N、P,氢化物为NH3、PH3,因NH3可以形成分子间氢键,故NH3的沸点高于PH3;
(4)Ca与H两种元素形成的化合物为离子化合物,化学式为CaH2,其中Ca最外层的两个电子分别转移到2个H上,Ca形成+2价离子,H形成-1价离子,故CaH2的电子式为![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某实验小组学生用50 mL 0.50 mol·L1盐酸与50 mL 0.55 mol·L1 NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量计算中和热。下列说法正确的是
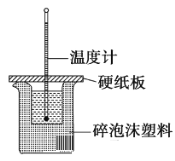
A. 实验过程中没有热量损失
B. 图中实验装置缺少环形玻璃搅拌棒
C. 烧杯间填满碎泡沫塑料的作用是固定小烧杯
D. 酸或碱的物质的量越大,所测中和热的数值越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,![]() 固体在
固体在![]() 溶液中的
溶液中的![]() 比在
比在![]() 中的
中的![]() 大
大
B.恒温恒容的密闭容器中,某储氢反应:![]() ,当容器内气体压强保持不变时,反应达到化学平衡
,当容器内气体压强保持不变时,反应达到化学平衡
C.铝-空气燃料电池,以![]() 溶液为电解液时负极反应为:
溶液为电解液时负极反应为:![]()
D.常温下,相同浓度的碳酸钠与碳酸氢钠的混合溶液中离子浓度的大小顺序为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭燃烧发电副产物可用于提取高纯度氧化铝,其工艺流程如下:
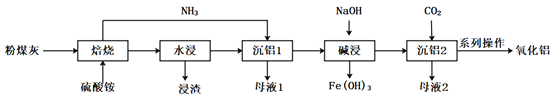
已知:粉煤灰的主要成份是Al2O3,主要杂质是SiO2、Fe2O3。
“焙烧”的主要反应:Fe2O3+4(NH4)2SO4=2NH4Fe(SO4)2+6NH3↑+3H2O Al2O3+4(NH4)2SO4=2NH4Al(SO4)2+6NH3↑+3H2O 回答下列问题:
(1)“浸渣”的主要成分为________(填化学式)。
(2)“沉铝1”中生成含铝元素沉淀的离子方程式是________。
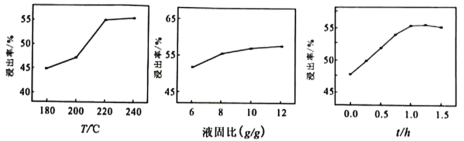
(3)结合下图分析“碱浸”时最优条件是________(填序号)。
A、200℃、8g/g、1.0h B、200℃、10g/g、1.5h C、220℃、10g/g、1.0h D、220℃、12g/g、1.5h
(4) “沉铝2”发生反应的离子方程式为________。
(5)流程中“一系列操作”是________。
(6)流程中可循环利用的物质是________。(填化学式)
(7)用1t含铝10.8%的粉煤灰,制得高纯度Al2O3 80kg,其产率为________%(结果保留1位小数)。
(8)传统工艺流程中第一步是将粉煤灰用硫酸“酸浸”脱硅,与之相比硫酸铵法的优点是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g)![]() CO2(g)+H2(g),在427 ℃时的平衡常数是9。如果反应开始时,一氧化碳和水蒸气的浓度都是0.01 mol/ L,计算一氧化碳在此反应条件下的转化率_____________。
CO2(g)+H2(g),在427 ℃时的平衡常数是9。如果反应开始时,一氧化碳和水蒸气的浓度都是0.01 mol/ L,计算一氧化碳在此反应条件下的转化率_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
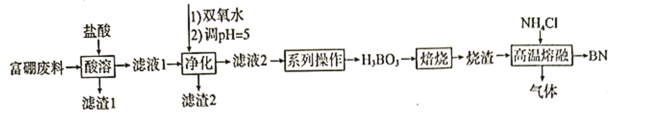
【题目】氮化硼![]() 广泛应用于制造合金、耐高温材料和半导体。科研小组以富硼废料(主要成分为
广泛应用于制造合金、耐高温材料和半导体。科研小组以富硼废料(主要成分为![]() 和
和![]() ,还含有少量
,还含有少量![]() 等)为原料,制备氮化硼的一种工艺流程如下:
等)为原料,制备氮化硼的一种工艺流程如下:
已知:硼酸溶于水和乙醇,在水中的溶解度如下
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度( | 2.77 | 4.78 | 8.90 | 14.89 | 23.54 | 39.60 |
回答下列问题:
(1)“酸溶”时需控制适当温度,温度不能过高的原因为____________________________;除控制适当温度外,可加快“酸溶”速率的措施还有__________________(答出一点即可)。
(2)“净化”时第一步反应的化学方程式为__________________;第二步调![]() 的目的为_______________;滤液2中
的目的为_______________;滤液2中![]() _______________(已知
_______________(已知![]() )
)
(3)“系列操作”中,洗涤结晶出来的硼酸的操作为__________________________。
(4)“高温熔融”过程中生成的气体为两种氢化物,则主要反应的化学方程式为__________________________;生成的气体用水吸收后可返回__________________________工序循环利用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M(![]() )是一种有机合成的中间体,下列关于M的说法正确的是( )
)是一种有机合成的中间体,下列关于M的说法正确的是( )
A.与苯互为同系物B.所有原子可能处于同一平面
C.二氯代物有16种(不含立体异构)D.![]() 燃烧最多消耗
燃烧最多消耗![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是
A.氨水应密闭保存,放置于低温处
B.对2HI(g) ![]() H2(g)+I2(g)平衡体系,增大平衡体系的压强可使气体颜色变深
H2(g)+I2(g)平衡体系,增大平衡体系的压强可使气体颜色变深
C.生产硝酸的过程中使用过量空气以提高氨气的利用率
D.溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1mol/L、体积分别为Va和Vb和的HX溶液与NH3·H2O溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法不正确的是( )
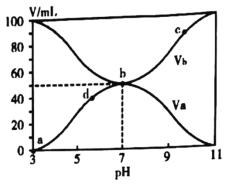
A.HX为弱酸
B.b点:![]()
C.b→c点过程中存在:![]()
D.c、d两点: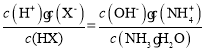 值相等
值相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com