
| A. | 原子核外的电子总是尽先排在能量高的电子层里,然后才排在能量低的电子层 | |
| B. | 某原子的核电荷数与最外层电子数相等 | |
| C. | 原子核外的电子层分为七层,每层所排的电子数相同 | |
| D. | 某原子M层上电子数是L层上电子数的4倍 |
分析 多电子原子中,原子核外电子根据能量不同,在不同区域内运动,即分层排布,能量低的电子在离核近的区域运动,能量高的电子在离核远的区域运动,据此分析.
解答 解:A、多个电子的原子里,电子是分层排布的,电子总是尽先排在能量低的电子层里,然后才排在能量高的电子层,故A错误;
B、原子的核电荷数与核外电子总数相等,当该原子只有一层即H和He时,原子的核电荷数与最外层电子数相等,故B正确;
C、核外的电子层分为七层,每层最多排的电子数为2n2,所以不同,故C错误;
D、核外电子每层最多排的电子数为2n2,并且电子电子是分层排布的,则M层上电子数不可能是L层上电子数的4倍,故错误;
故选B.
点评 本题考查了原子结构,核外电子排布规律及应用,熟悉电子离核的位置与能量的关系是解答的关键,较简单.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 将pH=4的CH3COOH溶液加水稀释10倍,溶液中各离子浓度均减小 | |
| B. | 用CH3COOH溶液滴定等物质的量浓度NaOH溶液至pH=7,V(CH3COOH)<V(NaOH)溶液 | |
| C. | 向0.2mol/L的盐酸溶液中加入等体积0.1mol•L-1的NH3•H2O溶液:c(Cl-)+c(OH-)=c(H+)+c(NH3•H2O) | |
| D. | 在含0.1mol NaHSO4溶液中:c(H+)=c(SO42-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnO4-、Fe2+、K+、Cl- | B. | Ca2+、Na+、Cl-、SO42- | ||
| C. | Ca2+、Cl-、NO3-、K+ | D. | Ca2+、H+、OH-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
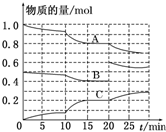 在恒定温度T℃,2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:
在恒定温度T℃,2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 117号元素位于第七周期第ⅦB族 | B. | 117号元素是一种金属元素 | ||
| C. | 117号元素最外层有5个电子 | D. | 117号元素没有正化合价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2OH→CH2=CH2↑+H2O | |
| B. | CH3CHBrCH3+NaOH→CH3CH=CH2↑+NaBr+H2O | |
| C. |  CHClCH2Cl+2NaOH→ CHClCH2Cl+2NaOH→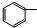 C≡CH+2NaCl+2H2O C≡CH+2NaCl+2H2O | |
| D. | 2CH3OH→CH3-O-CH3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锗是一种金属性很强的元素 | B. | 锗化氢(GeH4)稳定性很强 | ||
| C. | 锗酸(H4GeO4)是难溶于水的强酸 | D. | 锗元素位于第四周期第ⅣA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该有机物的分子式为CH4 | B. | 该有机物中含碳元素和氢元素 | ||
| C. | 该有机物中只含有碳元素和氢元素 | D. | 该有机物的化学性质比较稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com