
【题目】下列离子组能在溶液中大量共存的是
A. Fe2+、H +、Na+、NO3-B. SiO32-、K+、Br-、H +
C. NH4+、Cl-、Mg2+、SO42-D. Na +、OH-、NH4+、I-
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】F、G均是常见的香料,可通过下列途径合成,合成路线如图: 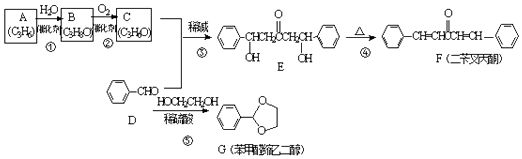
回答下列问题
(1)B的名称为 .
(2)③的反应类型是;④的反应类型是 .
(3)C的结构简式是;A加聚产物的结构简式是 .
(4)F分子中位于同一平面的碳原子最多有个.
(5)G的芳香同分异构体中且能发生银镜反应和水解反应的异构体有种,其中核磁共振氢谱只有四组峰的异构体结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是( )
A.纯碱可用于去除餐具的油污
B.“火树银花”中的焰火实质上是金属元素的焰色反应
C.碳酸钡可用于胃肠X射线造影检查
D.煤经过气化、液化等化学变化过程,可以转化为清洁能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)26H2O的流程如图1: 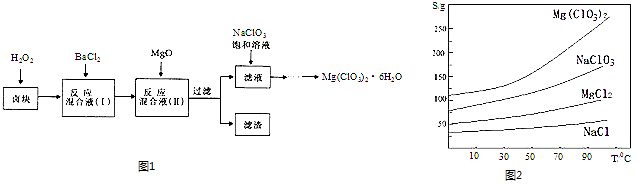
已知:①卤块主要成分为MgCl26H2O,含有MgSO4、FeCl2等杂质.
②四种化合物的溶解度(S)随温度(T)
变化曲线如图2所示.回答下列问题:
(1)过滤时主要的玻璃仪器有 .
(2)加入BaCl2的目的是除去杂质离子,检验已沉淀完全的方法是 .
(3)加速卤块在H2O2溶液中溶解的措施有:(写出一条即可)
(4)加入MgO的作用是; 滤渣的主要成分为 .
(5)向滤液中加入NaClO3饱和溶液后,发生反应的化学方程式为:MgCl2+2NaClO3=Mg(ClO3)2↓+2NaCl,再进一步制取Mg(ClO3)26H2O的实验步骤依次为①;②趁热过滤;③;④过滤、洗涤、干燥.
(6)产品中Mg(ClO3)26H2O含量的测定: 步骤1:准确称量3.50g产品配成100mL溶液.
步骤2:取10.00mL于锥形瓶中,加入10.00mL稀硫酸和20.00mL 1.000molL﹣1的FeSO4溶液,微热.
步骤3:冷却至室温,用0.l000molL﹣1K2Cr2O7溶液滴定剩余的Fe2+至终点,此过程中反应的离子方程式为:Cr2O72﹣+6Fe2++14H+=2Cr3++6Fe3++7H2O.
步骤4:将步骤2、3重复两次,计算得平均消耗K2Cr2O7溶液15.00mL.
①请写出步骤2中发生反应的离子方程式(还原产物为Cl﹣)
②产品中Mg(ClO3)26H2O的质量分数为 . (计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )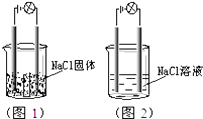
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl溶液中水电离出大量的离子
D.NaCl在水溶液中电离出了可以自由移动的离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是(设NA表示阿伏加德罗常数的值)( ) 
A.反应前气体的总体积为0.448L
B.装置中氢元素的总质量为0.04g
C.生成物中含有0.01NA个分子
D.生成物完全溶于水后所得溶液含有0.01 NA个NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气在工农业生产中有非常重要的应用.
(1)工业上常用氨气和醋酸二氨和铜{[Cu(NH3)2]Ac}的混合液来吸收一氧化碳(醋酸根CH3COO﹣简写为Ac﹣).反应方程式为:[Cu(NH3)2]Ac+CO+NH3[Cu(NH3)3CO]Ac ①请写出基态Cu原子的电子排布式 .
②氨水溶液中各元素原子的电负性从大到小排列顺序为 .
③醋酸分子中的两个碳原子,甲基(﹣CH3)碳和羧基(﹣COOH)碳的杂化方式分别是 .
④生成物[Cu(NH3)3CO]Ac中所含化学键类型有 .
a.离子键 b.配位键 c.σ键 d.π键
(2)如图为一个金属铜的晶胞,请完成以下各题. ①铜原子采取的这种堆积方式的空间利用率为 . (填数值)
②此晶胞立方体的边长为acm,Cu的相对原子质量为64.若阿伏伽德罗常数为NA , 则金属铜的晶体密度ρ为g/cm3 . (用a、NA表示).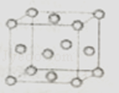
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列进行的各反应中,在反应过程中既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键生成的是
A.2NaBr+Cl2=2NaCl+Br2 B.2AgOH=Ag2O+H2O
C.2Na+2H2O=2NaOH+H2↑ D.2Na2O2+2H2O=4NaOH+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.05mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质.有关结论正确的是( )
加入的物质 | 结论 | |
A | 50mL 1mol/L H2SO4 | 反应结束后,c(Na+)=c(SO42﹣) |
B | 0.5mol CaO | 溶液中 |
C | 50mL H2O | 由水电离出的c(H+)c(OH﹣)不变 |
D | 0.1mol NaHSO4固体 | 反应完全后,溶液pH减小,c (Na+)不变 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com