
���� ��1���Ʊ�¶�ڿ����к�������Ӧ���������ƶ��䰵���ݴ�д����Ӧ�Ļ�ѧ����ʽ��
��2�����۳�С��˵���ƺ�ˮ�ų�������ʹ���ۻ����Ƶ��۵㽵�ͣ��Ƶ��ܶ�С��ˮ���Ƶ��۵�ϵͣ��ƺ�ˮ��Ӧ�����������ƺ������ҷų��������ƺ�ˮ��Ӧ�����������ƺ����������ŷ�Ӧ�Ľ���ˮ�������٣�����������Һ��Ϊ��������Һ����Һ�����������������ƣ���Ϊ���������ƵĴ��ڣ������������Ƶ��ܽ⣻
��3������ˮ��Ӧ�����������ƺ�����������������ת�Ƶ���֮��Ĺ�ϵʽ���㣻
��4�����ܺ�������ˮ��Ӧ����ú�Ͳ���Ӧ���ܶȴ���ú�ͣ�
��� �⣺��1���Ʒ����ڿ����к�������Ӧ���������ƶ��䰵����Ӧ����ʽΪ��4Na+O2�T2Na2O��
�ʴ�Ϊ���ƿ����������ɫ��Ϊ����ɫ�����ƿ����䰵����4Na+O2�T2Na2O��
��2�����۳�С��˵���ƺ�ˮ�ų�������ʹ���ۻ���ͬʱ˵���Ƶ��۵�ϵͣ�
A���ƺ�ˮ��Ӧ���������������ܹ۲쵽���ʴ���
B���Ƶ��۵�ϵ����ƺ�ˮ��Ӧ�ų���������ʹ���۳�С�������ܹ۲쵽���ʴ���
C���ƵĻ����Դ����ƣ����ơ��ƶ���ˮ��Ӧ���ɼ�����Ʋ������û����ƣ������н��������ɣ�����ȷ��
D����Ϊ�в�������������������Һ������Һ�����Կ�����Һ����ǣ��ʴ���
��ѡC��
�ʴ�Ϊ������ˮ��Ӧ�ų��������Ƶ��۵�ͣ�C��
��3������ˮ��Ӧ�����������ƺ����������ӷ���ʽ��2Na+2H2O=2Na++2OH-+H2�������ݷ���ʽ��֪������1mol����ת��2mol���ӣ������ɱ�״����224mL��H2�����ʵ���Ϊ0.01mol��ת�Ƶ�����Ϊ0.02mol��
�ʴ�Ϊ��2Na+2H2O=2Na++2OH-+H2����0.02mol��
��4����������֪�����ܺ�������ˮ��Ӧ����ú�Ͳ���Ӧ�����Ƶ��ܶȴ���ú�ͣ������ƿ��Ա�����ú�����Ը���������ˮ��
�ʴ�Ϊ��������������е�������ˮ�����ĽӴ���
���� ���⿼�����Ƶ����ʣ���ȷ�Ƶ��������ʺͻ�ѧ���ʣ�����ƺ�ˮ��Ӧ�����Ƶ������ǽ���ؼ���ע���ƺͱ�������������Һ��Ӧ�����������Ƶ��ܽ�������¶ȵ����߶����ͣ�Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ̬HBr�����磬���HBr�Ƿǵ���� | |
| B�� | ǿ�������Һ�ĵ����Բ�һ����ǿ | |
| C�� | NH3��ˮ��Һ�ܵ��磬���NH3�ǵ���� | |
| D�� | ǿ�������Һ̬ʱһ���ܵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | CH3CHO | C�� | CH3COOH | D�� | CH2=CH-COOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ܷ���ˮ�ⷴӦ | |
| B�� | �����������Ի���������·���ˮ����Ƶ÷��� | |
| C�� | ��������Һ�У�����Ũ���������Һ�г�����������ˮ������ܽ� | |
| D�� | ȡ����������Һ���Թ��У���������ϡ���ᣬ����3��5min������ȴ���μ�4��6��������ͭ����Һ���۲������ֺ�ɫ�������Ӷ��жϵ����Ƿ�����ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ƺ�ˮ��Ӧ��2Na2O2+2 H2O=4Na++4OH-+O2�� | |
| B�� | ��������������������Һ��Al2O3+2 OH-=2AlO2-+H2�� | |
| C�� | ����������Һ����ϡ�����У�Ba2++OHһ+H++SO42-=BaSO4��+H2O | |
| D�� | ������̼ͨ����������������Һ��CO2+OH-=HCO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 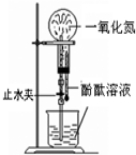 ��Ȫʵ�� | B�� | 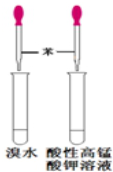 ��֤�����Ƿ���̼̼˫�� | ||
| C�� | 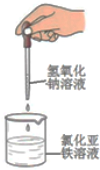 �Ʊ����������� | D�� | 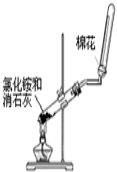 ʵ������ȡ���ռ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HClO3 | B�� | CaCl2 | C�� | Cl2O7 | D�� | Cl2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��1L1mol/L��NaCl��Һ��ȡ��500 ml����Ũ����0.5mol/L | |
| B�� | �Ƴ�0.5L10mol/L�����ᣬ��Ҫ�Ȼ�������112L����״���� | |
| C�� | 0.5L 2mol/LBaCl2��Һ�У�Ba2+��Cl-����Ϊ3��6.02��1023 | |
| D�� | 10g 98%���ᣨ�ܶ�Ϊ1.84g/cm3����1OmL 18.4mol/L�����Ũ������ͬ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com