
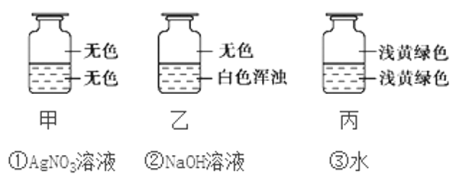
”¾ĢāÄæ”æĻņŹ¢ÓŠCl2µÄČżøö¼ÆĘųĘæ¼×”¢ŅŅ”¢±ūÖŠø÷×¢ČėĻĀĮŠŅŗĢåÖŠµÄŅ»ÖÖ,¾¹żÕńµ“,ĻÖĻóČēĻĀĶ¼ĖłŹ¾,Ōņ¼×”¢ŅŅ”¢±ū֊עČėµÄŅŗĢå·Ö±šŹĒ
A. ¢Ś¢Ł¢Ū B. ¢Ł¢Ś¢Ū
C. ¢Ū¢Ś¢Ł D. ¢Ł¢Ū¢Ś
”¾“š°ø”æA
”¾½āĪö”æ
ĀČĘųĪŖ»ĘĀĢÉ«ĘųĢ壬ÄÜČÜÓŚĖ®£¬ČÜÓŚĖ®µĆµ½ĀČĖ®£¬ĀČĖ®ŅņĪŖČܽāĀČĘųĻŌĒ³»ĘĀĢÉ«£»ĀČĘųÄܹ»ÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĀČ»ÆÄĘ”¢“ĪĀČĖįÄĘŗĶĖ®£»ĀČĘųÓėĖ®·“Ӧɜ³ÉŃĪĖįŗĶ“ĪĀČĖį£¬ŃĪĖįÓėĻõĖįŅų·“Ӧɜ³ÉĀČ»ÆŅų°×É«³Įµķ£¬¾Ż“Ė½ā“š”£
ĀČĘųĪŖ»ĘĀĢÉ«ĘųĢ壬ÄÜČÜÓŚĖ®£¬ČÜÓŚĖ®µĆµ½ĀČĖ®£¬ĀČĖ®ŅņĪŖČܽāĀČĘųĻŌĒ³»ĘĀĢÉ«£¬Čżøö¼ÆĘųĘæÖŠÖ»ÓŠ±ūŃÕÉ«ĪŖĒ³»ĘĀĢÉ«£¬ĖłŅŌ±ūÖŠŅŗĢåĪŖĖ®£»ĀČĘųÓėĖ®·“Ӧɜ³ÉŃĪĖįŗĶ“ĪĀČĖį£¬ŃĪĖįÓėĻõĖįŅų·“Ӧɜ³ÉĀČ»ÆŅų°×É«³Įµķ£¬¼×ŗĶŅŅÖŠ£¬Ö»ÓŠŅŅ³öĻÖĮĖ°×É«µÄ³Įµķ£¬ĖłŅŌŅŅÖŠŅŗĢåĪŖĻõĖįŅųČÜŅŗ£»ĀČĘųÄܹ»ÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĀČ»ÆÄĘŗĶ“ĪĀČĖįÄĘŗĶĖ®£¬ĖłŅŌĀČĘų±»ĒāŃõ»ÆÄĘĪüŹÕ£¬ČÜŅŗĪŖĪŽÉ«£¬¹Ź¼×ÖŠŅŗĢåĪŖĒāŃõ»ÆÄĘČÜŅŗ£¬Ōņ¼×”¢ŅŅ”¢±ū×¢ČėµÄŅŗĢå·Ö±šŹĒ¢Ś¢Ł¢Ū£»“š°øŃ”A”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææĘѧ¼ŅøÕøÕ·¢ĻÖĮĖijÖÖŌŖĖŲµÄŌ×Ó£¬1øöøĆŌ×ÓÖŹĮæŹĒa g£¬Ņ»øö12CŌ×ÓÖŹĮæŹĒb g£¬NAŹĒ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
¢ŁøĆŌ×ÓµÄĻą¶ŌŌ×ÓÖŹĮæĪŖ12a/b ¢Śm gøĆŌ×ÓµÄĪļÖŹµÄĮæĪŖ m/aNAmol
¢ŪøĆŌ×ÓµÄĦ¶ūÖŹĮæŹĒaNA g ¢ÜWgøĆŌ×ÓÖŠŗ¬ÓŠW/aøöøĆŌ×Ó
¢ŻÓÉŅŃÖŖŠÅĻ¢æÉµĆ£ŗNA=12/a
A. ¢Ł¢Ś¢Ü B. ¢Ł¢Ū C. ¢Ś¢Ū D. ¢Ū¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖij“æ¼ī£ØNa2CO3£©ŹŌŃłÖŠŗ¬ÓŠNaClŌÓÖŹ£¬ĪŖ²ā¶ØŹŌŃłÖŠ“æ¼īµÄÖŹĮæ·ÖŹż£¬æÉÓĆĻĀĶ¼ÖŠµÄ×°ÖĆ½ųŠŠŹµŃ锣
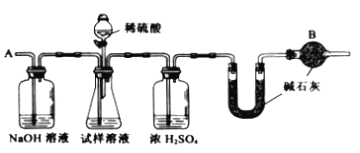
Ö÷ŅŖŹµŃé²½ÖčČēĻĀ£ŗ
¢Ł°“Ķ¼×é×°ŅĒĘ÷£¬²¢¼ģ²é×°ÖƵÄĘųĆÜŠŌ£»
¢Ś½«a gŹŌŃł·ÅČė׶ŠĪĘæÖŠ£¬¼ÓŹŹĮæÕōĮóĖ®Čܽā£¬µĆµ½ŹŌŃłČÜŅŗ£»
¢Ū³ĘĮæŹ¢ÓŠ¼īŹÆ»Ņ£ØCaOÓėNaOH¹ĢĢå»ģŗĻĪļ£©µÄUŠĶ¹ÜµÄÖŹĮ棬³ĘµĆĪŖb g£»
¢Ü“Ó·ÖŅŗĀ©¶·µĪČė6 mol”¤L-1 µÄĮņĖį£¬Ö±µ½²»ŌŁ²śÉśĘųĢåŹ±ĪŖÖ¹£»
¢Ż“Óµ¼¹ÜA“¦»ŗ»ŗ¹ÄČėŅ»¶ØĮæµÄæÕĘų£»
¢ŽŌŁ“Ī³ĘĮæŹ¢ÓŠ¼īŹÆ»ŅµÄUŠĶ¹ÜµÄÖŹĮ棻
¢ßÖŲø“²½Öč¢ŻŗĶ¢ŽµÄ²Ł×÷£¬Ö±µ½UŠĶ¹ÜµÄÖŹĮæ»ł±¾²»±ä£¬×īÖÕ³ĘµĆĪŖc g£»
ĒėĢīæÕŗĶ»Ų“šĪŹĢā£ŗ
£Ø1£©×°ÖĆÖŠøÉŌļ¹ÜBµÄ×÷ÓĆŹĒ__________________________________________
£Ø2£©²½Öč¢ŻµÄÄæµÄŹĒ__________________________________________________
£Ø3£©²½Öč¢ßµÄÄæµÄŹĒ__________________________________________________
£Ø4£©øĆŹŌŃłÖŠ“æ¼īµÄÖŹĮæ·ÖŹżµÄ¼ĘĖćŹ½ĪŖ___________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNAĪŖ°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ±ź×¼×“æöĻĀ£¬11.2 LµÄĪģĶéĖłŗ¬µÄ·Ö×ÓŹżĪŖ0.5 NA
B. ĻÖÓŠŅŅĻ©”¢±ūĻ©”¢¶”Ļ©µÄ»ģŗĻĘųĢå¹²14 g£¬ĘäŌ×ÓŹżĪŖ3 NA
C. 1 mol¼×»łµÄµē×ÓŹżÄæĪŖ7 NA
D. 28 gŅŅĻ©Ėłŗ¬¹²ÓƵē×Ó¶ŌŹżÄæĪŖ4 NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŅ»¶ØĮæÓŠ»śĪļŗĶ×ćĮæNa·“Ó¦µĆµ½![]() LĒāĘų£¬Č”ĮķŅ»·ŻµČĪļÖŹµÄĮæµÄĶ¬ÖÖÓŠ»śĪļŗĶ×ćĮæNaHCO3·“Ó¦µĆ
LĒāĘų£¬Č”ĮķŅ»·ŻµČĪļÖŹµÄĮæµÄĶ¬ÖÖÓŠ»śĪļŗĶ×ćĮæNaHCO3·“Ó¦µĆ![]() L¶žŃõ»ÆĢ¼£¬ČōŌŚĶ¬ĪĀĶ¬Ń¹ĻĀ
L¶žŃõ»ÆĢ¼£¬ČōŌŚĶ¬ĪĀĶ¬Ń¹ĻĀ![]() £½
£½![]() ”Ł0£¬ŌņøĆÓŠ»śĪļæÉÄÜŹĒ
”Ł0£¬ŌņøĆÓŠ»śĪļæÉÄÜŹĒ
¢ŁCH3CH(OH)COOH ¢ŚHOOC”ŖCOOH
¢ŪCH3CH2COOH¢ÜHOOCCH2CH(OH)CH2COOH”” ¢ŻCH3CH(OH)CH2OH
A. ¢Ś B. ¢Ś¢Ū¢Ü C. Ö»ÓŠ¢Ü D. ¢Ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCl2ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ ĀČĘų¼«ĘäĻą¹Ų²śĘ·ŌŚÉś²śÉś»īÖŠÓ¦ÓĆ¹ć·ŗ”£½įŗĻĀČĘųµÄĻą¹ŲÖŖŹ¶½ā¾öĻĀĮŠĪŹĢā£»
£Ø1£©ÓÉÓŚĀČĘųÖü“ęŌĖŹä²»·½±ć£¬¹¤ŅµÉĻ³£½«ĀČĘų×Ŗ»ÆĪŖĘÆ°×·Ū£¬¹¤ŅµÉĻÉś²śĘÆ°×·ŪµÄÖ÷ŅŖ»Æѧ·½³ĢŹ½ŹĒ______________________£»ĘÆ°×·ŪµÄÓŠŠ§³É·ÖŹĒ£ØĢī»ÆѧŹ½£©_________”£ĘÆ°×·ŪŌŚæÕĘųÖŠ³¤ĘŚ“ę·Å»į±äÖŹ¶ųŹ§Š§µÄŌĄķŹĒ£ØÓĆ»Æѧ·½³ĢŹ½ĖµĆ÷£© _____________”£
£Ø2£©ŹµŃéŹŅæÉÓƶžŃõ»ÆĆĢŗĶÅØŃĪĖį·“Ó¦ÖĘČ”ĀČĘų£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ MnO2+4HCl(ÅØ) ![]() MnCl2+Cl2”ü+2H2O ÓÉÓŚĀČĘųÓŠ¶¾ĖłŅŌŹµŃéŹŅĶس£ÓĆ___________________ČÜŅŗĪüŹÕĪ²Ęų£ØĢī»ÆѧŹ½£©£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____________________”£
MnCl2+Cl2”ü+2H2O ÓÉÓŚĀČĘųÓŠ¶¾ĖłŅŌŹµŃéŹŅĶس£ÓĆ___________________ČÜŅŗĪüŹÕĪ²Ęų£ØĢī»ÆѧŹ½£©£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____________________”£
£Ø3£©ĀČĘųŹĒŅ»ÖÖ³£ÓƵÄĻū¶¾¼Į£¬ŠĀÖĘĀČĖ®ŗ¬¶ąÖÖĪ¢Į£²¢±ķĻÖ³ö²»Ķ¬µÄŠŌÖŹ(ÓĆ»ÆѧŹ½»ņĄė×Ó·ūŗÅĢīŠ“)£ŗ
Ź¹ĀČĖ®³Ź»ĘĀĢÉ«µÄŹĒ________£»ÄÜŹ¹AgNO3ČÜŅŗ²śÉś°×É«³ĮµķµÄŹĒ________£»ÄÜŹ¹×ĻÉ«ŹÆČļŹŌŅŗĻŌŗģÉ«µÄŹĒ________£»ÄÜŹ¹ŗģÖ½ĶŹÉ«µÄŹĒ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°“ŅŖĒó»Ų“š£ŗ
(1)Fe2O3+2Al![]() Al2O3+2Fe£¬ŌŚøĆ·“Ó¦ÖŠ________ŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøß,øĆŌŖĖŲµÄŌ×Ó____µē×Ó£ØµĆµ½»ņŹ§Č„£©,_____________ŹĒŃõ»Æ¼Į,______________ŹĒ»¹Ō¼Į,________ŹĒ»¹Ō²śĪļ,________ŹĒŃõ»Æ²śĪļ”££ØĢī»ÆѧŹ½£©
Al2O3+2Fe£¬ŌŚøĆ·“Ó¦ÖŠ________ŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøß,øĆŌŖĖŲµÄŌ×Ó____µē×Ó£ØµĆµ½»ņŹ§Č„£©,_____________ŹĒŃõ»Æ¼Į,______________ŹĒ»¹Ō¼Į,________ŹĒ»¹Ō²śĪļ,________ŹĒŃõ»Æ²śĪļ”££ØĢī»ÆѧŹ½£©
(2)±ź³öĻĀĮŠ»ÆŗĻĪļÖŠÖø¶ØŌŖĖŲµÄ»ÆŗĻ¼Ū”£
KMnO4ÖŠMnŌŖĖŲµÄ»ÆŗĻ¼Ū__________£¬KClO3ÖŠClŌŖĖŲµÄ»ÆŗĻ¼Ū__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓÉĻĀĮŠŹµŃé¼°ĻÖĻóĶĘ³öµÄĻąÓ¦½įĀŪÕżČ·µÄŹĒ
Ń”Ļī | ŹµŃé | ĻÖĻó | ½įĀŪ |
A | 2 mL0.01mol”¤L-1µÄKIČÜŅŗÖŠµĪČėµČĢå»żµČÅØ¶ČµÄFeCl3ČÜŅŗ£¬½«³ä·Ö·“Ó¦ŗóµÄČÜŅŗ·ÖČż·Ż£¬Ņ»·ŻµĪČėK3[Fe(CN)6]ČÜŅŗ£¬µŚ¶ž·ŻµĪČėKSCNČÜŅŗ£¬µŚČż·ŻµĪČėµķ·ŪČÜŅŗ | µĪČėK3[Fe(CN)6]ČÜŅŗŗó²śÉśĄ¶É«³Įµķ£»µĪČėKSCNČÜŅ¹ŗó±äŃŖŗģÉ«£»µĪČėµķ·ŪČÜŅŗŗóČÜŅŗ±äĄ¶ | KIČÜŅŗŗĶFeCl3ČÜŅŗ·¢Éś·“Ó¦£ŗ2Fe3++2I- |
B | ĻņĻ”ĮņĖįÖŠ¼ÓČėĶʬ£¬Č»ŗóĶØČėŃõĘų¼ÓČČ | ĻČĪŽĆ÷ĻŌĻÖĻó£¬ĶØČėŃõĘų¼ÓČČŗóČÜŅŗ±äĄ¶ | Ńõ»ÆŠŌ£ŗĻ”ĮņĖį>Cu2+ |
C | ĻņÅØ¶Č¾łĪŖ0.1 mol”¤L-1µÄNa2SO3ŗĶNa2SiO3ČÜŅŗÖŠ·Ö±šµĪ¼Ó·ÓĢŖ | Na2SiO3ČÜŅŗŗģÉ«øüÉī | ·Ē½šŹōŠŌ£ŗSi<S |
D | ½«¼øµĪµČÅØ¶ČµÄFeCl3ČÜŅŗ”¢AlCl3ČÜŅŗĶ¬Ź±µĪČė×ćĮæµČÅØ¶ČµÄNaOHČÜŅŗÖŠ | Ö»²śÉśŗģŗÖÉ«³Įµķ | Ksp[Al(OH)3]>K sp[Fe(OH)3] |
A. A B. B C. C D. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»ÖÖĶ»ĘĘ“«Ķ³µē³ŲÉč¼ĘĄķÄīµÄĆ¾-ĢąŅŗĢ¬½šŹō“¢Äܵē³ŲµÄ¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£¬øƵē³ŲĖłÓĆŅŗĢåĆÜ¶Č²»Ķ¬£¬ŌŚÖŲĮ¦×÷ÓĆĻĀ·ÖČż²ć£¬¹¤×÷Ź±ÖŠ¼ä²ćČŪČŚŃĪµÄ×é³É¼°ÅØ¶Č²»±ä”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©

A. ·ÅµēŹ±£¬Mg£ØŅŗ£©²ćµÄÖŹĮæ¼õŠ”
B. ·ÅµēŹ±Õż¼«·“Ó¦ĪŖMg2++2e-=Mg
C. øƵē³Ų³äµēŹ±£¬Mg-Sb£ØŅŗ£©²ć·¢Éś»¹Ō·“Ó¦
D. øƵē³Ų³äµēŹ±£¬Cl-ĻņÖŠĻĀ²ć½ēĆꓦŅʶÆ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com