

| ||
| ||
| ||
| △ |
| ||
| △ |
| n |
| V |
| ||||
|
| 1 |
| Vm |
| ||
| ||
| n |
| V |
| ||||
|
| 1 |
| Vm |
| 1 |
| 22.4 |
| ||
| △ |
| ||
| △ |
| n |
| V |
| ||||
|
| 1 |
| Vm |


科目:高中化学 来源: 题型:阅读理解
| ||
| 高温高压 |
| ||
| 高温高压 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源: 题型:
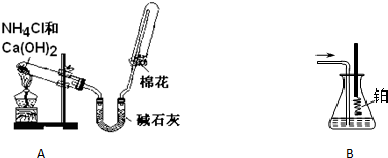
某同学用如下实验装置及化学药品制取氨气并研究氨气的催化氧化。请你按要求回答下列问题:


A B
(1)该同学制取氨气的化学方程式为 。
(2)检验氨气是否收集满的方法是(简述操作方法、现象和结论)_________________。
(3)一段时间后,将收集氨气的试管倒立在水槽中,观察到试管内液面最终只上升到试管的一半。若不考虑试管内溶质扩散到水槽中,则标准状况下,试管内溶液的物质的量浓度为 。
(4)用B装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入B装置的锥形瓶内,写出锥形瓶内氨氧化的化学方程式 。
(5)反应结束后锥形瓶内的溶液中含有H+、OH-、 、 离子。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省德州市陵县一中高三(上)期中化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com