
| A. | Cl-、Mg2+、H+、K+ | B. | Na+、Ba2+、OH-、SO42- | ||
| C. | Ag+、K+、Cl-、SO42一 | D. | MnO4-、NO3-、SO42-、Na+ |
分析 与NH4HCO3作用能产生气体,为酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水、弱电解质等,不能发生氧化还原反应等,则离子大量共存,并结合离子的颜色来解答.
解答 解:与NH4HCO3作用能产生气体,为酸或强碱溶液,
A.酸溶液中该组离子之间不反应,可大量共存,且离子均为无色,故A选;
B.Ba2+、SO42-结合生成沉淀,一定不能共存,故B不选;
C.Ag+分别与Cl-、SO42-结合生成沉淀,一定不能共存,故C不选;
D.MnO4-为紫色,与无色不符,故D不选;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
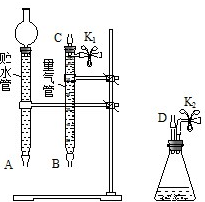 某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.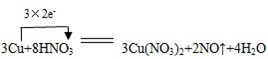 .
.| 实验编号 | 稀硝酸的浓度 /(mol/L) | 稀硝酸的体积 /mL | 温度 /℃ | 时间 /min | 收集气体的体积/mL |
| ① | a | V | 25 | t1 | V1 |
| ② | V | ||||
| ③ | V |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应①中(C6H10O5)n可表示淀粉或纤维素 | |
| B. | 反应②属于氧化反应 | |
| C. | 将在空气中灼烧后的铜丝趁热插入乙醇中可得到乙酸 | |
| D. | 反应③得到的乙酸乙酯中含有乙醇和乙酸,可用饱和氢氧化钠溶液除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲表示A、B 两物质的溶解度随温度变化情况,将tl℃时A、B 的饱和溶液分别升温至t2℃时(水不减少),溶质的质量分数B>A | |
| B. | 乙表示常温下,稀释HA、HB 两种酸的稀溶液时,溶液pH 随加水量的变化,则NaA 溶液的pH 小于同浓度的NaB 溶液的pH | |
| C. | 丙表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ•mol-1 | |
| D. | 丁表示恒温恒容条件下,2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A 对应的状态为化学平衡状 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将气体通入澄清石灰水 | B. | 将气体通入到氢氧化钠溶液中 | ||
| C. | 将气体通入到石蕊溶液中 | D. | 将气体通入到酸性高锰酸钾溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3与盐酸 | B. | Cl2与NaOH溶液 | C. | Na2O2和CO2 | D. | Na2S2O3与稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
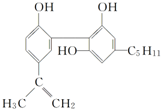 我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构简式如图:
我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构简式如图:| A. | 它的化学式为C20H24O3 | |
| B. | 从结构上看,它属于酚类 | |
| C. | 从结构上看,它属于醇类 | |
| D. | 从元素组成上看,它可以在氧气中燃烧生成CO2和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com