
科目:高中化学 来源: 题型:选择题
| A. | 危险化学品危害人类健康,应禁止生产 | |
| B. | 金属钠可以保存在石蜡油中,并贴上 标志 标志 | |
| C. | 可以用大量水扑灭爆炸引发的大火 | |
| D. | 硝酸铵、氰化钠、电石和金属钠均属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
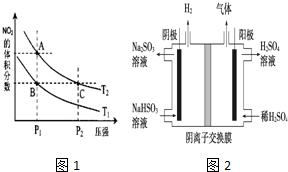
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②③④ | C. | ②③④⑥ | D. | ①②③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
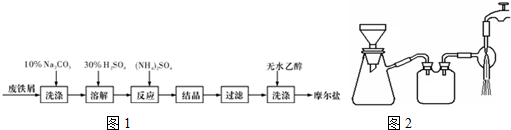
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 以下均为中学化学常见物质,存在如下转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.
以下均为中学化学常见物质,存在如下转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2=Cu2++2 OH- | B. | NH3•H2O?NH4++OH- | ||
| C. | HF=H++F- | D. | H3PO43?3H++PO43- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com