
【题目】40℃时,在氨-水体系中不断通入CO2,各种离子的变化趋势如下图所示,不正确的是( )
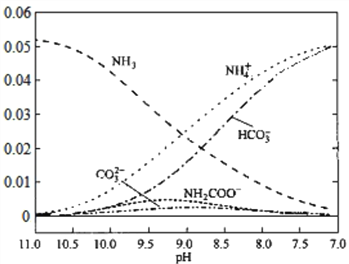
A. 在pH=9.0时,c(NH4+)>c(HCO3ˉ)>c(NH2COOˉ)>c(CO32-)
B. 在氨-水体系中不断通入CO2,体系中始终存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3ˉ)+c(OHˉ)
C. 随着CO2的通入,![]() 不断减小
不断减小
D. pH=7时,水的电离程度最大
科目:高中化学 来源: 题型:
【题目】需要配制500 mL 0.5 mol·L-1氢氧化钠溶液,经测定实际所配氢氧化钠溶液的浓度为0.45 mol·L-1。可能的原因是( )
A. 转移时溶液没有冷却至室温 B. 容量瓶没有烘干
C. 称量氢氧化钠固体时砝码放反了 D. 定容时仰视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)100mL0.2mol/L Na2SO4溶液中含有SO42﹣___________________mol,Na+的物质的量浓度是_________________mol/L。
(2)5molCO2在标准状况下所占的体积约为________L;所含氧原子的数目约为_______个。
(3)3.01×1023个OH﹣的物质的量为___mol,质量为______g,含有电子的物质的量为_______mol,这些OH﹣与___________mol NH3的质量相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中得到的粗食盐水中常含Ca2+、Mg2+、SO42—,需要分离提纯。现有含少量CaCl2、MgCl2、Na2SO4的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂:①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中的Ca2+、Mg2+、SO42—。提纯时的操作步骤和加入试剂的情况如图。
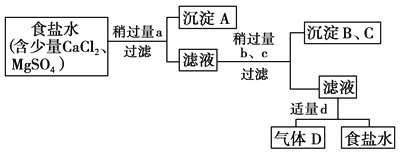
图中a、b、c、d分别表示上述4种试剂中的一种。若a为BaCl2溶液,请回答:
(1)沉淀A的是________。(填化学式)
(2)过滤操作需要的玻璃仪器有___________________________。
(3)试剂d是________;判断试剂d已经过量的方法是:________________________。
(4)加入b、c后溶液中发生的化学反应的化学方程式有:MgCl2 + 2NaOH == Mg(OH)2 ↓ + 2NaCl;
____________________________________________ ;_________________________________。
(5)检验粗食盐水中含有SO42—的方法是___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃D是一种重要的化工原料且在标准状况下的密度为1.25 gL1,E能发生银镜反应,C与乙酸、乙醇均发生酯化反应且分子中含有甲基。有关物质的转化关系如下图所示。
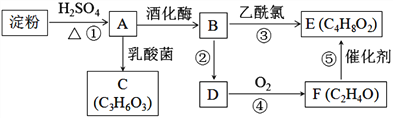
(1)A中所含官能团的名称为________________。
(2)C的结构简式为________________。
(3)已知乙酰氯的结构简式为![]() ,反应③的化学方程式为_________________。
,反应③的化学方程式为_________________。
(4)下列说法正确的是________。
A.判断反应①是否完全,可用碘水检验
B.两分子C发生酯化反应生成环状的酯
C.一定条件下,A、B、C、E都能与NaOH反应
D.反应⑤为加成反应,也属于酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去KCl溶液中少量的MgCl2、MgSO4,从稀盐酸、Na2CO3、Ba(NO3)2、K2CO3、Ba(OH)2溶液中,选择A、B、C 3种试剂,按图中的实验步骤进行操作:
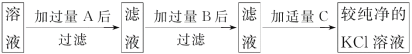
(1)3种试剂的化学式:A______,B______,C______。
(2)加过量A的原因是___________________________________________________________,有关反应的化学方程式为________________________________________________________________。
(3)加过量B的原因是______________________________________________________,有关反应的化学方程式为_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,![]() ,
,![]() ,
,![]() ,下列说法正确的是
,下列说法正确的是
A. ![]() 与
与![]() 等体积混合后的溶液中:
等体积混合后的溶液中:![]()
B. 用相同浓度的![]() 溶液分别滴定等体积pH均为3的HCOOH和
溶液分别滴定等体积pH均为3的HCOOH和![]() 溶液至终点,消耗
溶液至终点,消耗![]() 溶液的体积相等
溶液的体积相等
C. ![]() 与
与![]() 盐酸等体积混合后的溶液中
盐酸等体积混合后的溶液中![]() :
: ![]()
D. 浓度均为![]() 的
的![]() 和
和![]() 溶液中阳离子的物质的量浓度之和: 前者小于后者
溶液中阳离子的物质的量浓度之和: 前者小于后者
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com