
| A£® | ¢Ś¢Ū¢Ż | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ł¢Ś¢Ū | D£® | ¢Ł¢Ś¢Ü¢Ż |
·ÖĪö PbO2µÄŃõ»ÆŠŌ±ČĀČĘųĒ棬æÉÓėÅØŃĪĖį·“Ӧɜ³ÉĀČĘų£¬ĀČĘų¾ßÓŠĒæŃõ»ÆŠŌ£¬Óė½šŹō·“Ó¦æÉÉś³É×īĪČ¶ØµÄĪļÖŹ£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗ¢ŁPb+2Cl2ØTPbCl4£¬Éś³ÉĪļPbCl4ÖŠPbĪŖ+4¼Ū£¬²»ĪČ¶Ø£¬¹Ź¢Ł“ķĪó£»
¢ŚSn+2Cl2ØTSnCl4£¬Éś³ÉĪļSnCl4ÖŠSnĪŖ+4¼Ū£¬ĪČ¶Ø£¬¹Ź¢ŚÕżČ·£»
¢ŪSnCl2+Cl2ØTSnCl4£¬SnCl2ÖŠSnĪŖ+2¼Ū²»ĪČ¶Ø£¬Äܹ»¼ĢŠų±»Ńõ»ÆĪŖ+4¼Ū£¬¹Ź¢ŪÕżČ·£»
¢ÜPbO2+4HCl=PbCl4+2H2O£¬PbCl4ÖŠPbĪŖ+4¼Ū£¬²»ĪČ¶Ø£¬¹Ź¢Ü“ķĪó£»
¢ŻPb3O4+8HClØT3PbCl2+Cl2”ü+4H2O£¬PbCl2ÖŠPbĪŖ+2¼Ū£¬ŹĒĪČ¶ØµÄ£¬¹Ź¢ŻÕżČ·£»
¹ŹŃ”£ŗA£®
µćĘĄ ±¾Ģāæ¼²éĮĖŃõ»Æ»¹Ō·“Ó¦µÄ¹ęĀÉ£¬×¼Č·°ŃĪÕĢāÄæøų³öĢõ¼žŹĒ½āĢā¹Ų¼ü£¬×¢Ņā²»Ķ¬¼ŪĢ¬Ģ¼×åŌŖĖŲµÄĪČ¶ØŠŌ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ēæµē½āÖŹČÜŅŗµÄµ¼µēŠŌŅ»¶Ø±ČČõµē½āÖŹČÜŅŗµÄµ¼µēŠŌĒæ | |
| B£® | Ź³ŃĪČÜŅŗÄܵ¼µē£¬ĖłŅŌĖüŹĒµē½āÖŹ | |
| C£® | NaHSO4ĪŽĀŪŌŚĖ®ČÜŅŗĄļ»¹ŹĒŌŚČŪȌדĢ¬ĻĀ¶¼æÉŅŌµēĄė³öNa+”¢H+ŗĶSO42- | |
| D£® | SO3µÄĖ®ČÜŅŗæÉŅŌµ¼µē£¬µ«Ėü²»ŹĒµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ł¢Ś¢Ū | C£® | ¢Ł¢Ś¢Ū¢Ü | D£® | ¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
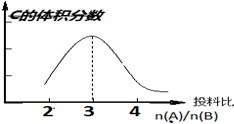 ŌŚŗćĪĀŗćŃ¹Ģõ¼žĻĀ£ŗaA£Øg£©+bB£Øg£©?2C£Øg£©£¬ŅŌ²»Ķ¬µÄĶ¶ĮĻ±ČæŖŹ¼·“Ó¦£¬·Ö±š“ļµ½Ę½ŗāŹ±£¬CµÄĢå»ż·ÖŹżÓėĶ¶ĮĻ±ČµÄ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ
ŌŚŗćĪĀŗćŃ¹Ģõ¼žĻĀ£ŗaA£Øg£©+bB£Øg£©?2C£Øg£©£¬ŅŌ²»Ķ¬µÄĶ¶ĮĻ±ČæŖŹ¼·“Ó¦£¬·Ö±š“ļµ½Ę½ŗāŹ±£¬CµÄĢå»ż·ÖŹżÓėĶ¶ĮĻ±ČµÄ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2+O2$?_{¼ÓČČ}^{“߻ƼĮ}$ 2SO 3”÷H=-196.6 kJ/mol | |
| B£® | H2£Øg£©+$\frac{1}{2}$O2£Øg£©ØTH2O£Ø l £©”÷H=-285.8 kJ/mol | |
| C£® | 2H2£Ø g £©+O2£Ø g £©ØT2H2O £Ø l £©”÷H=+571.6 kJ/mol | |
| D£® | C£Øs£©+O2£Ø g £©ØTCO2£Øg£©”÷H=+393.5 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | MgCl2¾§Ģå | B£® | ČŪČŚµÄKOH | C£® | ŅŗĢ¬HCl | D£® | NaClČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
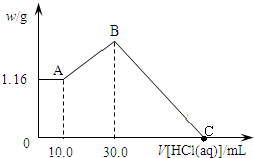
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
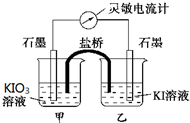 ½«·“Ó¦IO3-+5I-+6H+?3I2+3H2OÉč¼Ę³ÉČēĶ¼ĖłŹ¾µÄŌµē³Ų£¬¼×”¢ŅŅÉÕ±ÖŠ¶¼¼ÓČėµķ·ŪČÜŅŗ£®æŖŹ¼Ź±Ļņ¼×ÉÕ±ÖŠ¼ÓČėÉŁĮæÅØĮņĖį£¬µēĮ÷¼ĘÖøÕė·¢ÉśĘ«×Ŗ£¬Ņ»¶ĪŹ±¼äŗ󣬵ēĮ÷¼ĘÖøÕė»Ųµ½Įć£¬ŌŁĻņ¼×ÉÕ±ÖŠµĪČė¼øµĪÅØNaOHČÜŅŗ£¬µēĮ÷¼ĘÖøÕėŌŁ“Ī·¢ÉśĘ«×Ŗ£®ĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ£Ø””””£©
½«·“Ó¦IO3-+5I-+6H+?3I2+3H2OÉč¼Ę³ÉČēĶ¼ĖłŹ¾µÄŌµē³Ų£¬¼×”¢ŅŅÉÕ±ÖŠ¶¼¼ÓČėµķ·ŪČÜŅŗ£®æŖŹ¼Ź±Ļņ¼×ÉÕ±ÖŠ¼ÓČėÉŁĮæÅØĮņĖį£¬µēĮ÷¼ĘÖøÕė·¢ÉśĘ«×Ŗ£¬Ņ»¶ĪŹ±¼äŗ󣬵ēĮ÷¼ĘÖøÕė»Ųµ½Įć£¬ŌŁĻņ¼×ÉÕ±ÖŠµĪČė¼øµĪÅØNaOHČÜŅŗ£¬µēĮ÷¼ĘÖøÕėŌŁ“Ī·¢ÉśĘ«×Ŗ£®ĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | Į½“ĪµēĮ÷¼ĘÖøÕėĘ«×Ŗ·½ĻņĻą·“£¬µēĮ÷¼Ę¶ĮŹżĪŖĮ揱£¬·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬ | |
| B£® | Į½“ĪŹµŃéÖŠ£¬ŃĪĒÅÖŠµÄŃōĄė×ÓŅĘ¶Æ·½ĻņĻą·“ | |
| C£® | æŖŹ¼¼ÓČėÉŁĮæÅØĮņĖįŹ±£¬Ö»ÓŠŅŅÉÕ±ÖŠČÜŅŗ±äĄ¶ | |
| D£® | Ļņ¼×ÉÕ±ÖŠµĪČė¼øµĪÅØNaOHČÜŅŗŗó£¬ŅŅÖŠŹÆÄ«µē¼«ÉĻ·¢Éś»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com