
现有常温时pH=1的某强酸溶液10 mL,下列操作能使溶液的pH变成2的是
| A.加水稀释成100 mL。 |
| B.加入10 mL的水进行稀释。 |
| C.加入10 mL 0.01 mol/L的NaOH溶液。 |
| D.加入10 mL 0.01 mol/L的HCl溶液。 |
科目:高中化学 来源: 题型:单选题
放射性元素碘131(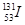 )和铯137(
)和铯137(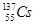 )是核反应物中的主要元素。下列叙述正确的是
)是核反应物中的主要元素。下列叙述正确的是
A.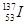 与 与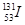 的所有性质都相同 的所有性质都相同 |
B.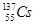 原子中含有中子数比质子数多27 原子中含有中子数比质子数多27 |
C.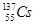 与 与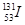 的中子数相同 的中子数相同 |
D.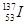 与 与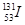 是同素异形体 是同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(16分)二甲醚是重要的有机中间体,利用二氧化碳加氢合成二甲醚能变废为宝,且可替代汽油作为新型清洁燃料。
(1)常温常压下,二氧化碳加氢可选择性生成二甲醚或一氧化碳:
①CO2 (g)+3H2(g)=CH3OH(l)+H2O(l) △H1 =-55.7 kJ/mol
②2CH3OH(l) = CH3OCH3(g)+H2O (l) △H2 =-23.4 kJ/mol
③CO2 (g)+3H2(g) =CO(g) + H2O (l) △H 3>0
则CO2(g)加氢转化为CH3OCH3(g)和H2O (l)的热化学方程式是___________________________________________________。
(2)合成二甲醚往往选用硅铝混合物作催化剂,硅铝比例不同,生成二甲醚或一氧化碳的物质的量分数不同。下图是硅铝比与产物选择性图:
反应③的平衡常数表达式为 ,图中A点和B点的平衡常数比较:KA______KB(填“>、=、<”)。根据以上两条曲线,写出其中一条变化规律: ___________________。
(3)在280oC时,向一个2L的密闭容器中加入等量2mol二氧化碳和氢气, A点二甲醚的浓度为0.15 mol·L-1,计算在A点二氧化碳的转化率,要求写出计算过程。
(4)二甲醚逐渐发展为替代汽油的清洁燃料,在二甲醚燃料电池中,二甲醚通入______极,碱性条件下,该电极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定温度下,当Mg(OH)2固体在水溶液中达到下列平衡时:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是:
Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是:
| A.加MgCl2 | B.加H2O | C.加NaOH | D.加HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
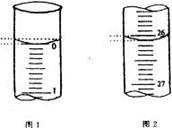
有一支50mL酸式滴定管其中盛有溶液,液面恰好在10mL刻度处,现把管内溶液全部流下排出,用量筒承接,该溶液的体积应为
| A.10mL | B.40mL | C.大于40mL | D.小于40ml |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,将下列物质溶于水中分别配制成0.1 mol?L—1溶液,所得溶液pH大于7的是
| A.NaCl | B.HCl | C.NaOH | D.CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(11分)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:(1)选用的指示剂是 。
(2)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视______________________。
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________。
| A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液 |
| B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
| 滴定次数 | 待测氢氧化钠溶液的体积/ mL | 0.1000 mol/L 盐酸的体积/ mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/ mL | ||
| 第一次 | 25.00 | | | |
| 第二次 | 25.00 | 2.00 | 28.08 | 26.08 |
| 第三次 | 25.00 | 0.22 | 26.34 | 26.12 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法不正确的是( )
| A.聚乙烯制成的塑料可以反复加热熔融,是热塑性材料 |
| B.用碱催化生成的酚醛树脂能形成网状结构,不溶于任何溶剂 |
| C.在制备高吸水性树脂时要加入交联剂,以得到具有网状结构的树脂 |
| D.通常说的三大合成材料是指塑料、合成纤维、合成洗涤剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com