
A、丙烷分子的比例模型: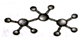 |
| B、乙醚的分子式为:C2H6O |
C、2-乙基-1,3-丁二烯分子的键线式: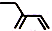 |
| D、化学名词:乙酸乙脂、苯、活性碳、钳锅 |
 ,故A错误;
,故A错误; ,故C正确;
,故C正确;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、17% | B、25% |
| C、33% | D、50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
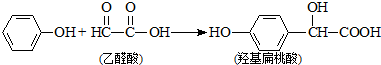
| A、该反应是加成反应 |
| B、上述反应的原子利用率可达到100% |
| C、乙醛酸与H2在热的镍催化下反应生成乙二醇 |
| D、对羟基扁桃酸可以发生加成反应、取代反应和缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 可判断可逆反应A2(g)+3B2(g)?2AB3(g)正反应是放热反应 可判断可逆反应A2(g)+3B2(g)?2AB3(g)正反应是放热反应 |
B、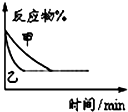 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
C、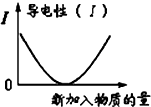 可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
D、 表示10mL 0.01 mol?L-1 KMnO4酸性溶液与过量的0.1mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 表示10mL 0.01 mol?L-1 KMnO4酸性溶液与过量的0.1mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaClO=Na++ClO- |
| B、H2CO3?2H++CO32- |
| C、NaHSO4═H++SO42-+Na+ |
| D、Al2(SO4)3=2Al3++3SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气通入水中:Cl2+H2O=2H++Cl-+ClO- |
| B、向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C、向Fe(NO3)2稀溶液中加入盐酸:Fe2++4H++NO3-=Fe3++NO↑+2H2O |
| D、向NaHCO3溶液中加入少量的Ba(OH)2溶液:Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、x=2 |
| B、2min内A的反应速率为0.6 mol?L-1?min-1 |
| C、B的转化率为40% |
| D、若混合气体的密度不变,则表明该反应达到平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com