
【题目】在一容积固定的密闭容器中,可逆反应H2(g)+I2(g) ![]() 2HI(g)达到平衡状态的标志是
2HI(g)达到平衡状态的标志是
A. 混合气体的密度保持不变
B. H2、I2、HI的分子数之比为1:1:2
C. 容器内混合气体的颜色不再发生变化
D. 1mol H—H键断裂的同时有2molH—I键形成
科目:高中化学 来源: 题型:
【题目】在电镀车间的含铬酸性废水中,铬的存在形式有Cr(Ⅵ)和Cr(Ⅲ)两种,其中以Cr(Ⅵ)的毒性最大。电解法处理含铬废水如图,铬最终以Cr(OH)3沉淀除去。下列说法正确的是
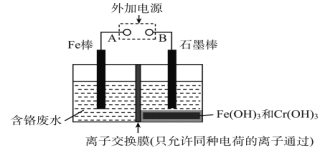
A. Fe为阳极,反应为Fe-2e-=Fe2+
B. 阴极反应为Cr2O72-+7H2O+6e-=2Cr(OH)3↓+8OH-
C. 阳极每转移3mol电子,可处理Cr(Ⅵ)物质的量为1mol
D. 离子交换膜为质子交换膜,只允许H+穿过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选择性催化还原法(SCR)烟气脱硝技术是一种成熟的NOx控制处理方法,主要反应如下:
①4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) △H1=akJ·mol-1
4N2(g)+6H2O(g) △H1=akJ·mol-1
②4NH3(g)+2NO2(g)+O2(g)![]() 3N2(g)+6H2O(g) △H2=bkJ·mol-1
3N2(g)+6H2O(g) △H2=bkJ·mol-1
副反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H4=dkJ·mol-1
4NO(g)+6H2O(g) △H4=dkJ·mol-1
可以计算出反应2NO(g)+O2(g)![]() 2NO2(g)的△H为( )
2NO2(g)的△H为( )
A. (4b-3a+d)/4 B. (4a-3b+d)/4 C. (3b-4a+d)/4 D. (3a-4b+d)/4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe2+、Ba2+、H+、SO42-、CO32-。为了进一步确认,对该溶液进行实验检测:

步骤一:仔细观察,该溶液呈无色、透明、均一状态。
步骤二:加入足量BaCl2溶液,生成23.3g 白色沉淀,再加稀硝酸,沉淀不消失。
(1)原溶液中除上图中的离子以外,肯定还含有的离子是________,肯定不含有的离子是________。
(2)实验操作的步骤二中称量沉淀前的实验操作步骤有:过滤、洗涤、______________、检验沉淀已洗干净的方法是____________。
(3)原溶液中H+物质的量浓度为_________mol/L。
(4)向原溶液中加入NaHCO3溶液,反应的离子方程式为_____________。
(5)若向100 mL原溶液中加入1mo/L 的Ba(OH)2溶液,当生成的沉淀质量刚好最大时,则加入的Ba(OH)2溶液体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定容积的密闭容器中,可逆反应: mA(气)+nB(气) ![]() pC(气)+qD(气),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化, ②体系的密度不再发生变化, ③各组分的物质的量浓度不再改变, ④各组分的质量分数不再改变,⑤反应速率vA:vB:vC:vD=m:n:p:q,其中,能说明反应已达到平衡的是
pC(气)+qD(气),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化, ②体系的密度不再发生变化, ③各组分的物质的量浓度不再改变, ④各组分的质量分数不再改变,⑤反应速率vA:vB:vC:vD=m:n:p:q,其中,能说明反应已达到平衡的是
A. ③④ B. ②③④ C. ①②③④ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X是某种药物的主要成分,工业上合成该化合物的一种路线如下(部分反应物、反应条件略去):

已知:酯与含羟基的化合物可发生如下酯交换反应:RCOO R′+R″OH![]() RCOOR″+R′OH(R、R′、R″均代表烃基)。
RCOOR″+R′OH(R、R′、R″均代表烃基)。
(1)反应①所需的试剂是_______,反应②的反应类型是_________。
(2)B中含氧官能团的名称是________;反应④的产物除了X以外,另一种产物的名称是________。
(3)D在一定条件下能发生缩聚反应生成高分子化合物,该高分子化合物的结构简式为____________。
(4)反应③的化学方程式为_______________________。
(5)E的同分异构体有多种,写出符合下列条件的有机物结构简式________。
Ⅰ.苯环上一氯代物只有一种
Ⅱ.与氯化铁溶液发生显色反应
Ⅲ.能与碳酸氢钠溶液反应放出CO2
(6)已知:①![]()
![]()
![]() ;②当苯环上已有一个“—CH3”或“—Cl”时,新引入的取代基一般在它的邻位或对位;当苯环上已有一个“—NO2”或“—COOH”时,新引入的取代基一般在它的间位。请写出以甲苯、乙醇为原料制备
;②当苯环上已有一个“—CH3”或“—Cl”时,新引入的取代基一般在它的邻位或对位;当苯环上已有一个“—NO2”或“—COOH”时,新引入的取代基一般在它的间位。请写出以甲苯、乙醇为原料制备 的合成路线图(无机试剂任用)____________。
的合成路线图(无机试剂任用)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钾是一种无色晶体,易溶于水,实验室制备KI晶体的步骤如下:
①在如图所示的三颈烧瓶中加入12.7g研细的单质碘和100mL1.5mol/L的KOH溶液,搅拌(已知:I2与KOH反应产物之一是KIO3)
②碘完全反应后,打开分液漏斗中的活塞和弹簧夹1、2.向装置C中通入足量的H2S;
③反应结束后,向装置C中加入稀H2SO4酸化,水浴加热
④冷却,过滤得KI粗溶液。

(1)仪器a的名称_________;
(2)A中制取H2S气体的化学方程式___________;
(3)B装置中饱和NaHS溶液的作用是_________(填序号);
①干燥H2S气体 ②除HCl气体
(4)D中盛放的试剂是__________;
(5)步骤①中发生反应的离子方程式是_____________;
(6)由步骤④所得的KI粗溶液(含SO42-),制备KI晶体的实验方案:边搅拌边向溶液中加入足量的BaCO3,充分搅拌、过滤、洗涤并检验后,将滤液和洗涤液合并,加入HI溶液调至弱酸性,在不断搅拌下蒸发至较多固体析出,停止加热,用余热蒸干,得到KI晶体,理论上,得到KI晶体的质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
I.已知某些化学键的键能数据如下
化学键 | C=O | C—O | C—H | H—H | O—H |
键能/kJ·mol-1 | 745 | 351 | 415 | 436 | 462 |
则CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) ΔH = __________ kJ·mol-1
CH3OH(g) + H2O(g) ΔH = __________ kJ·mol-1
II.将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g) + 6H2(g)![]() CH3OCH3(g) + 3H2O(l)
CH3OCH3(g) + 3H2O(l)
(1)该反应化学平衡常数表达式K = __________。
(2)已知在某压强下,该反应在不同温度、不同投料比时,达平衡时CO2的转化率如图所示:

①该反应的ΔH __________ 0(填“>"或“<”)。
②若温度不变,减小反应投料比[n(H2)/n(CO2)],K值将____(填“增大”、“减小”或“不变”)。
(3)某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生上述反应,下列物理量不再发生变化时,能说明反应达到平衡状态的是__________。
A.二氧化碳的浓度 B.容器中的压强
C.气体的密度 D.CH3OCH3与H2O的物质的量之比
(4)某温度下,在体积可变的密闭容器中,改变起始时加入各物质的量,在不同的压强下,平衡时CH3OCH3(g)的物质的量如下表所示:
P1 | P2 | P3 | |
I.2.0 mol CO2 6.0 mol H2 | 0.10 mol | 0.04 mol | 0.02 mol |
II.1.0 mol CO22 | X1 | Y1 | Z1 |
III.1.0 mol CH3OCH3 3.0 mol H2O | X2 | Y2 | Z2 |
①P1 __________ P3(填“>”“<”或“=”);
②P2下,III中CH3OCH3的平衡转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列叙述正确的是( )

A. 反应开始到10 s,用Z表示的反应速率为0.158 mol·L-1·s-1
B. 10 s后,该反应停止进行
C. 反应的化学方程式为2X(g)+Y(g)![]() 2Z(g)
2Z(g)
D. 0~10 s的时间内的平均反应速率:v(X)=v(Y)=0.0395 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com