
 4NO+6H2O。请从下图中选用所需的仪器(可重复使用)组成一套进行该反应的简单装置。现提供试剂:过氧化钠、碱石灰、铂粉、氯化钙、浓硫酸、浓氨水和氢氧化钠溶液。
4NO+6H2O。请从下图中选用所需的仪器(可重复使用)组成一套进行该反应的简单装置。现提供试剂:过氧化钠、碱石灰、铂粉、氯化钙、浓硫酸、浓氨水和氢氧化钠溶液。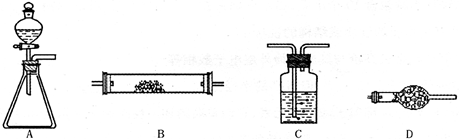
| 选用的仪器(填字母) | 加入的试剂 | 作用 |
| | | |
| | | |
| | | |
| | | |
| 选用的仪器(填字母) | 加入的试剂 | 作用 |
| A | 分液漏斗:浓氨水 锥形瓶:过氧化钠(或Na2O2) | 提供反应物 (或其他合理叙述) |
| D | 碱石灰 | 干燥混合气体 (或其他合理叙述) |
| B | 铂粉 | 反应的催化剂 (或其他合理叙述) |
| C(D) | 氢氧化钠溶液(碱石灰) | 吸收氮的氧化物,防止污染空气(或其他合理叙述) |
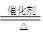 4NO+6H2O。原料必须要提供氧气和氨气,原料中能提供氧气和氨气的应该是浓氨水和过氧化钠反应,仪器是装置A;出来后的气体因为有水蒸气,必须用干燥剂除去,但是因为有氨气,不能选用浓硫酸,只能用碱石灰,选择装置D;在B中进行氨的催化氧化,用到催化剂铂粉;产生的氮氧化物要用氢氧化钠溶液吸收,选择装置C,如果用碱石灰,则选择装置D。
4NO+6H2O。原料必须要提供氧气和氨气,原料中能提供氧气和氨气的应该是浓氨水和过氧化钠反应,仪器是装置A;出来后的气体因为有水蒸气,必须用干燥剂除去,但是因为有氨气,不能选用浓硫酸,只能用碱石灰,选择装置D;在B中进行氨的催化氧化,用到催化剂铂粉;产生的氮氧化物要用氢氧化钠溶液吸收,选择装置C,如果用碱石灰,则选择装置D。

 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.50mL |
| 第二次 | 0.20mL | 18.80mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
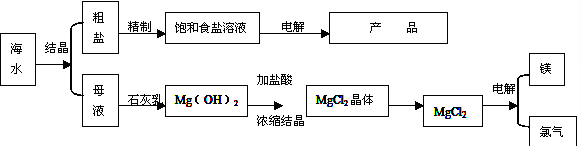
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
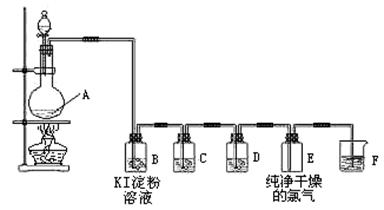
 MnCl2+C12↑+2H2O,在方程式上标出电子转移的方向和数目;该反应的氧化剂是 ;
MnCl2+C12↑+2H2O,在方程式上标出电子转移的方向和数目;该反应的氧化剂是 ;查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 2BN + 3H2O。(已知:BN高温下能被空气氧化,不溶于水;B2O3难溶于冷水但可溶于热水。)
2BN + 3H2O。(已知:BN高温下能被空气氧化,不溶于水;B2O3难溶于冷水但可溶于热水。)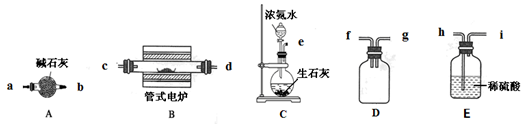
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com