
| A�� | 1mol O2��g��������һ������2mol SO2��g�������� | |
| B�� | 2mol SO2��g����1mol O2��g����������һ������2mol SO3��g���������� | |
| C�� | 2mol SO2��g��������һ������2mol SO3��g�������� | |
| D�� | ��÷�ӦΪ���ȷ�Ӧ���ʲ��ؼ��ȾͿɷ��� |
���� ���ڷ��ȷ�Ӧ����Ӧ���������������������������������ȷ�Ӧ����Ӧ��������С�����������������еķ��ȷ�Ӧ��Ҫ���Ȳ��ܷ������ݴ˽��н��
��� �⣺��Ӧ 2SO2+O2�T2SO3Ϊ���ȷ�Ӧ������2mol SO2��g����1mol O2��g����������һ������2mol SO3��g��������������A��C����B��ȷ��
���ܸ÷�Ӧ�Ƿ��ȵģ������ڸ����²��ܷ�������D����
��ѡB��
���� ���⿼�������������ͷ�Ӧ�ȵĹ�ϵ����Ŀ�Ѷ��еȣ��������Ҫ��ȷ��Ӧ��������ָ��Ӧ�����������������������ָ���������������ͣ�������ijһ����Ӧ���ijһ���������������жԱȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
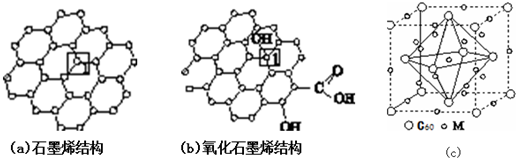
 ���DZ�C60Լ��20��ϳɳ���һ�ֶԳ���������ӣ���������Ѻϳɳ�һ����������C60�ĸ����ͷ��Ӿ��壬�þ���ľ����ṹ��ͼ��d����ʾ����������������ԭC60����ķ��Ӽ��϶�У���ø����ͷ��Ӿ��������ö��ߵķ���ʽ�ɱ�ʾΪC8H8��C60
���DZ�C60Լ��20��ϳɳ���һ�ֶԳ���������ӣ���������Ѻϳɳ�һ����������C60�ĸ����ͷ��Ӿ��壬�þ���ľ����ṹ��ͼ��d����ʾ����������������ԭC60����ķ��Ӽ��϶�У���ø����ͷ��Ӿ��������ö��ߵķ���ʽ�ɱ�ʾΪC8H8��C60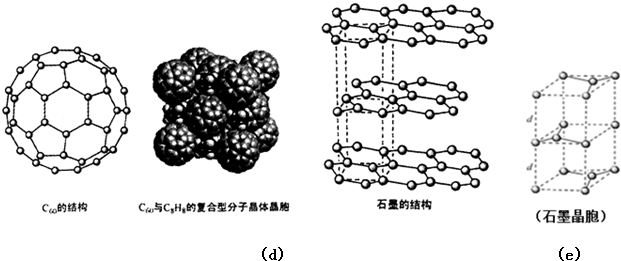
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
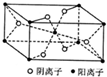 X��Y��Z��RΪǰ������Ԫ�أ���ԭ��������������XY2���γ��������Ҫ����֮һ��Z��̬ԭ�ӵ�M����K���������ȣ�R2+��3d�����9�����ӣ���ش��������⣺
X��Y��Z��RΪǰ������Ԫ�أ���ԭ��������������XY2���γ��������Ҫ����֮һ��Z��̬ԭ�ӵ�M����K���������ȣ�R2+��3d�����9�����ӣ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
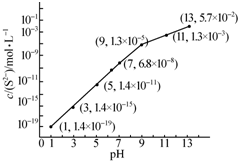 �о���Ԫ�ؼ��仯��������ʾ�����Ҫ���壮
�о���Ԫ�ؼ��仯��������ʾ�����Ҫ���壮| Ka1 | Ka2 | |
| H2SO3 | 1.3��10-2 | 6.3��10-4 |
| H2CO3 | 4.2��10-7 | 5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | x+10 | B�� | x+26 | C�� | x-34 | D�� | x-24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
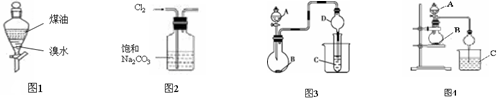 ��������
��������| A�� | ����ͼ1��ɡ���ú������ȡ��ˮ�е�Br2����������ã��ϲ��Ⱥ�ɫ���²㼸����ɫ | |
| B�� | ʵ������ȡ����Cl2������ͼ2װ�ó�ȥCl2�е�HCl�������� | |
| C�� | ͼ3�У���A��B��C�ֱ�ΪŨ���ᡢNa2SO3���塢ʯ����Һ����C����Һ�ȱ�����ɫ | |
| D�� | ͼ4�У���AΪŨ��ˮ��BΪ��ʯ�ң�C������ϡ��Һ��ʵ���пɿ���C���ȱ���Ǻ����壬˵��AgOH�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
| �� �� | �� Ʒ | ����ϡ�������� | ��Ӧ����Һ���� |
| ������g�� | 9 | 75.4 | 80 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
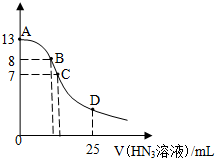 ��������25mL0.1mol•L-1 NaOH��Һ����εμ�0.2mol•L-1��HN3��Һ�������ᣩ��pH�ı仯������ͼ��ʾ����Һ���ʱ����ı仯���Բ��ƣ��������Ka=10-4.7��������˵����ȷ���ǣ�������
��������25mL0.1mol•L-1 NaOH��Һ����εμ�0.2mol•L-1��HN3��Һ�������ᣩ��pH�ı仯������ͼ��ʾ����Һ���ʱ����ı仯���Բ��ƣ��������Ka=10-4.7��������˵����ȷ���ǣ�������| A�� | A��ˮ�������c��H+��С��B�� | |
| B�� | ��B�㣬����Ũ�ȴ�СΪ c��OH-����c��H+����c��Na+����c��N3-�� | |
| C�� | ��C�㣬�μӵ�V��HN3��=12.5mL | |
| D�� | ��D�㣬c��H+����10-4.7 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com