
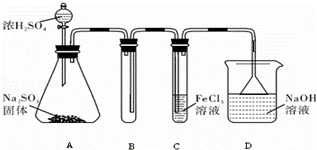
某研究小组用下图装置进行SO2 与FeCl3溶液反应的相关实验(夹持装置已略去).
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在 中,再加水稀释,这样操作的目的是 ,操作中不需要的仪器有 (填字母).
a.药匙 b.烧杯 c.石棉网 d.玻璃棒 e.坩埚
(2)通入足量SO2时C中观察到的现象为 ,
(3)根据以上现象,该小组同学认为SO2 与 FeCl3溶液发生氧化还原反应.
①写出SO2与FeCl3溶液反应的离子方程式 ;
②请设计实验方案检验有Fe2+生成取 ;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42﹣.该做法 (填“合理”或“不合理”),理由是 .
(4)D装置中倒置漏斗的作用是 .
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有 (填入正确选项前的字母).
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液.
考点: 性质实验方案的设计;实验装置综合.
专题: 实验设计题.
分析: (1)配制氯化铁溶液时,应加相应的酸抑制铁离子水解,在烧杯中稀释配制溶液;
(2)通入足量SO2时C中发生二氧化硫与氯化铁的氧化还原反应,生成硫酸亚铁;
(3)①发生氧化还原反应,生成硫酸根离子、亚铁离子;
②检验有Fe2+生成,利用KSCN和氯水,先不变红,后变红分析;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,硝酸具有强氧化性;
(4)倒置漏斗可防止NaOH溶液倒吸;
(5)验证SO2具有还原性,选择与二氧化硫反应的具有强氧化性的物质.
解答: 解:(1)配制氯化铁溶液时,需先把氯化铁晶体溶解在浓盐酸中,再加水稀释,这样操作的目的是抑制铁离子水解,操作中需要用药匙取固体在烧杯中进行溶解,用利用玻璃棒不断搅拌,不需要的仪器有c、e,
故答案为:浓盐酸;抑制氯化铁水解;c、e;
(2)通入足量SO2时C中发生二氧化硫与氯化铁的氧化还原反应,生成硫酸亚铁,则观察到溶液由棕黄色变为浅绿色,故答案为:溶液由棕黄色变为浅绿色;
(3)①发生氧化还原反应,生成硫酸根离子、亚铁离子,离子反应为2Fe3++SO2+2H2O=SO42﹣+4H++2Fe2+,故答案为:2Fe3++SO2+2H2O=SO42﹣+4H++2Fe2+;
②检验有Fe2+生成的实验方法为取C中反应后的溶液,向其中滴入KSCN溶液,不变红,再加入新制的氯水,溶液变红,
故答案为:取C中反应后的溶液,向其中滴入KSCN溶液,不变红,再加入新制的氯水,溶液变红;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,硝酸具有强氧化性,则硝酸可以将溶解的SO2氧化为 H2SO4,干扰试验,故做法不合理,
故答案为:不合理;硝酸可以将溶解的SO2氧化为 H2SO4,干扰试验;
(4)因尾气易溶于NaOH溶液,则倒置漏斗的作用为防止NaOH溶液倒吸,故答案为:使气体充分吸收,防止溶液倒吸;
(5)验证SO2具有还原性,可与高锰酸钾或碘水发生氧化还原反应,S元素的化合价升高,而与浓硫酸、NaCl不反应,故答案为:b、c.
点评: 本题考查性质实验方案的设计及实验装置综合,为高频考点,把握装置中发生的反应及氧化还原反应原理的应用为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
一定温度和压强下,30L某种气态纯净物中含有6.02×1023个分子,这些分子由1.204×1024个原子组成,下列有关说法中不正确的是( )
|
| A. | 标准状况下该纯净物若为气态,其体积约是22.4 L |
|
| B. | 该气体中每个分子含有2个原子 |
|
| C. | 若O2在该条件下为气态,则1 mol O2在该条件下的体积也为30 L |
|
| D. | 该温度和压强可能是标准状况 |
查看答案和解析>>
科目:高中化学 来源: 题型:
二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等.它的结构如图所示,下列说法正确的是( )

|
| A. | 二茂铁中Fe2+与环戊二烯离子(C5H5﹣)之间为离子键 |
|
| B. | 1mol环戊二烯中含有σ键的数目为5NA |
|
| C. | 分子中存在π键 |
|
| D. | Fe2+的电子排布式为1s22s22p63s23p63d44s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
无水氯化铝是一种重要韵催化剂,工业上由Al2O3制备无水氯化铝的反应为:2Al2O3(s)+6Cl2(g) 4AlCl3(g)+3O2(g)△H>0.下列分析错误的是()
4AlCl3(g)+3O2(g)△H>0.下列分析错误的是()
A. 增大反应体系的压强,反应速率可能加快
B. 加入碳粉,平衡向右移动,原因是碳与O2反应,降低了生成物的浓度且放出热量
C. 电解熔融的Al2O3和AlCl3溶液均能得到单质铝
D. 将AlCl3•6H2O在氯化氢气流中加热,也可制得无水氯化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是()
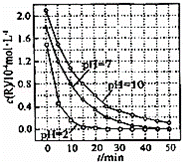
A. 在0﹣50min之间,pH=2和pH=7 时R的降解百分率相等
B. 溶液酸性越强,R 的降解速率越小
C. R的起始浓度越小,降解速率越大
D. 在 20﹣25min之间,pH=10 时 R 的平均降解速率为 0.04mol•L﹣1•min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气是一种重要的工业原料.工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气.下列说法错误的是( )
|
| A. | 若管道漏气遇氨就会产生白烟 |
|
| B. | 该反应利用了Cl2的强氧化性 |
|
| C. | 该反应属于复分解反应 |
|
| D. | 生成1mol N2有6mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
运用元素周期律分析下面的推断,其中不正确的是( )
|
| A. | 锂(Li)与水反应比钠与水反应剧烈 |
|
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 |
|
| C. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 |
|
| D. | HBrO4的酸性比HIO4的酸性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在298K时下述反应的有关数据:
C(s)+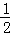 O2(g)=CO(g)△H1=﹣110.5kJ/mol
O2(g)=CO(g)△H1=﹣110.5kJ/mol
C(s)+O2(g)=CO2(g),△H2=﹣393.5kJ/mol
则C(s)+CO2(g)=2CO(g)的△H 为( )
A. 283.5kJ/mol B. 172.5kJ/mol C. ﹣172.5kJ/mol D. ﹣504 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
“三鹿奶粉”事件波及很广,据调查某些奶农为了提高鲜奶的“蛋白质”含量,往里面加了点三聚氰胺C3H6N6(见右图),三聚氰胺可由尿素合成.下列说法错误的是( )
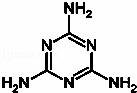
A. 尿素是人工合成的第一种有机物
B. 三聚氰胺不是芳香族化合物
C. 三聚氰胺属于氨基酸
D. 饮用含三聚氰胺的奶粉会导致肾结石
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com