
 如图是一些常见元素的单质或化合物之间的转化关系.溶液中的水以及部分反应物或生成物未标出.A、E是空气中的两种主要成分,C是由两种元素组成的新型材料,并且C的原子数、最外层电子数之和与SiC相同,J是一种能引起温室效应的气体,K是两性化合物.反应③、④、⑤用于工业中生产H.
如图是一些常见元素的单质或化合物之间的转化关系.溶液中的水以及部分反应物或生成物未标出.A、E是空气中的两种主要成分,C是由两种元素组成的新型材料,并且C的原子数、最外层电子数之和与SiC相同,J是一种能引起温室效应的气体,K是两性化合物.反应③、④、⑤用于工业中生产H. ,G的化学式NO;
,G的化学式NO;分析 A、E是空气中的两种主要成分,分别为O2、N2中的一种,A与B反应得到C、SiC与D,由元素守恒可知B中至少含有Si、C元素,D与E反应得到J是一种能引起温室效应的气体,则J为CO2,C与氢氧化钠溶液反应得到F与I,I与J反应得到两性化合物K与钠盐,则K为Al(OH)3,则B中含有Si、C、Al三种元素,C是由两种元素组成的新型材料,并且C的原子数、最外层电子数之和与SiC相同,则C为AlN,故A为N2,D为碳,E为O2,F为NH3,I为NaAlO2,由转化关系可知G为NO,反应③、④、⑤用于工业中生产H,应为氨的催化氧化,工业制硝酸的反应,所以H为HNO3,据此解答.
解答 解:A、E是空气中的两种主要成分,分别为O2、N2中的一种,A与B反应得到C、SiC与D,由元素守恒可知B中至少含有Si、C元素,D与E反应得到J是一种能引起温室效应的气体,则J为CO2,C与氢氧化钠溶液反应得到F与I,I与J反应得到两性化合物K与钠盐,则K为Al(OH)3,则B中含有Si、C、Al三种元素,C是由两种元素组成的新型材料,并且C的原子数、最外层电子数之和与SiC相同,则C为AlN,故A为N2,D为碳,E为O2,F为NH3,I为NaAlO2,由转化关系可知G为NO,反应③、④、⑤用于工业中生产H,应为氨的催化氧化,工业制硝酸的反应,所以H为HNO3.
(1)A为N2,电子式为 ,G的化学式为:NO,
,G的化学式为:NO,
故答案为: ;NO;
;NO;
(2)D和H反应的化学方程式:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2+↑+2H2O,
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2+↑+2H2O;
(3)反应⑥为二氧化碳与偏铝酸钠的反应,反应离子方程式为CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-,
故答案为:CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-;
(4)B中含有Al、Si、C等元素,Si与另外两种元素的物质的量之比均为1:4,则B为Al4SiC4,与氮气反应生成AlN、SiC和C,反应的方程式为:Al4SiC4+2N2$\frac{\underline{\;1500℃\;}}{\;}$4AlN+SiC+3C,
故答案为:Al4SiC4+2N2$\frac{\underline{\;1500℃\;}}{\;}$4AlN+SiC+3C.
点评 本题考查无机物的推断,侧重于学生的分析能力的考查,注意利用“物质结构特点、性质、J为温室效应气体、K为两性化合物:等B为突破口进行推断,难度中等.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ | |
| B. | 氢氧燃料电池的负极反应式:O2+4H++4e-═2H2O | |
| C. | 粗铜精炼时,与电源正极相连是纯铜,电极反应式为Cu-2e-═Cu2+ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
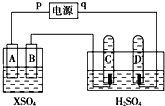 如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡,试回答:
如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Si→SiO2→H2SiO3→Na2SiO3 | B. | Al→Al2O3→Al(OH)3→NaAl(OH)4 | ||
| C. | N2→NH3→NO→NO2→HNO3→NO2 | D. | S→SO3→H2SO4→SO2→Na2SO3→Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
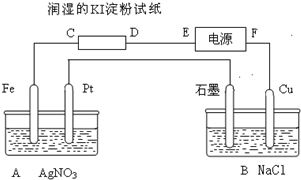 有电解装置如图所示.图中A装置盛1L 2mol/L AgNO3溶液.通电后,润湿的淀粉KI试纸的C端变蓝色,电解一段时间后试回答:
有电解装置如图所示.图中A装置盛1L 2mol/L AgNO3溶液.通电后,润湿的淀粉KI试纸的C端变蓝色,电解一段时间后试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质的最外层电子数都是7 | |
| B. | 卤素单质与H2化合的容易程度为F2<Cl2<Br2<I2 | |
| C. | 卤素单质与H2化合的产物由上至下稳定性减弱,其水溶液的酸性增强 | |
| D. | 从F到I,元素非金属性依次减弱,则其最高价氧化物的水化物的酸依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同 | |
| B. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| C. | 在加热条件下发生的反应均为吸热反应 | |
| D. | 物质发生化学反应时不一定都伴随着能量变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com