
 某温度下,在2L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示.
某温度下,在2L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示.分析 (1)根据参加反应的物质的物质的量之比等于化学计量数之比书写化学方程式;
(2)根据v=$\frac{△c}{△t}$计算;
(3)根据判断反应速率大小,5min后物质的物质的量不变说明反应达到平衡状态,所以反应速率不变;
(4)影响反应速率的因素分析,降低温度反应速率减小;
(5)反应是气体体积减小的放热反应,当达到平衡时,正逆反应速率相同,各组分含量保持不变,及其衍生的定量关系.
解答 解:(1)由图象可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质的量增多,应为生成物,
当反应进行到5min时,△n(Y)=0.2mol,△n(Z)=0.4mol,△n(X)=0.6mol,
则△n(Y):△n(Z):△n(X)=1:2:3,参加反应的物质的物质的量之比等于化学计量数之比,
则反应的方程式为:3X+Y?2Z,故答案为:3X+Y?2Z;
(2)反应开始至2min末,Z的反应速率为:v=$\frac{△c}{△t}$=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/(L•min),故答案为:0.05mol/(L•min);
(3)图象分析可知,反应到5min后,物质的量 不再发生变化,说明反应达到平衡状态,所以5min后Z的生成速率和5min末Z的生成速率相同,故答案为:等于;
(4)影响反应速率的因素分析,降低温度反应速率减小,故答案为:减小;
(5)a.气体质量和体积不变,无论该反应是否达到平衡状态,容器内密度始终不变,所以混合气体的密度不再变化不能判断平衡状态,故a错误;
b.该反应是一个反应前后气体体积减小的可逆反应,当容器内压强保持不变时,正逆反应速率相等,反应达到平衡状态,混合气体的压强不再变化说明反应达到平衡状态,故b正确;
c.同一物质的正反应速率等于逆反应速率说明达到化学平衡状态,故c正确;
d.各组分浓度不变达到化学平衡状态,所以X的浓度保持不变说明达到化学平衡状态,故d正确;
e.生成1molZ和同时生成1.5molX,说明正逆反应速率相等,即达到化学平衡状态,故e正确;
f.各组分反应速率之比等于其化学计量数之比,故X、Y、Z的反应速率之比为3:1:2,故f错误,
故答案为:af.
点评 本题主要考查了平衡状态的判断、反应速率的计算、气体压强之比等于物质的量之比等知识点,中等难度,掌握基础是关键.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:选择题
| A. | 硫酸生产中常采用催化剂提高SO2的转化率 | |
| B. | 合成氨中采用及时分离氨气提高反应速率 | |
| C. | 电镀铜时,溶液中c(Cu2+)基本保持不变 | |
| D. | 用电解熔融氧化镁的方法制取镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
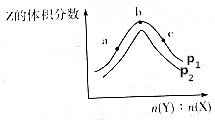 一定温度下,某密闭容器中存在反应:X(g)+2Y(g)?2Z(g),测得平衡体系中Z的体积分数与体系的压强(p)、投料比[b(Y):n(X)]关系如图所示,下列分析一定正确的是( )
一定温度下,某密闭容器中存在反应:X(g)+2Y(g)?2Z(g),测得平衡体系中Z的体积分数与体系的压强(p)、投料比[b(Y):n(X)]关系如图所示,下列分析一定正确的是( )| A. | p2>p1 | B. | Y的转化率:a<c<b | ||
| C. | b点时n(Y):n(X)=2 | D. | 该反应是一个放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组别 | 草酸的体积(mL) | 温度 | 其他物质 |
| ① | 2Ml | 20 | 无 |
| ② | 2mL | 20 | 10滴饱和MnS04溶液 |
| ③ | 2mL | 30 | 无 |
| ④ | 1mL | 20 | 1mL蒸馈水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用氨水除去试管内壁上的银镜 | |
| B. | 利用乙酸乙酯和乙醇的密度不同,可用分液的方法分离 | |
| C. | 用燃烧法鉴别乙醇、苯和四氯化碳 | |
| D. | 用氢氧化钠溶液鉴别乙醇、乙酸和乙酸乙酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com