
 ��2�֣�
��2�֣� ��
�� ��2.5����
��2.5����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Ӧ����������Na2O2����ԭ����FeSO4 |
| B������2 mol Na2FeO4ʱ����Ӧ�й���8 mol����ת�� |
| C��Na2FeO4�������Դ���Na2O2 |
| D��Na2FeO4��ˮ�����У�����������ԭ��Ӧ���������з�������ԭ��Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
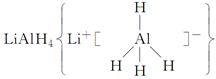 ��LiH���ǽ���������������л��ϳ��еij����Լ�����ˮ���ܾ��ҷ�Ӧ�ų�H2��LiAlH4��125 ��ֽ�ΪLiH��H2��Al������˵���в���ȷ���� (����)��
��LiH���ǽ���������������л��ϳ��еij����Լ�����ˮ���ܾ��ҷ�Ӧ�ų�H2��LiAlH4��125 ��ֽ�ΪLiH��H2��Al������˵���в���ȷ���� (����)��| A��LiH��D2O��Ӧ������������Ħ������Ϊ4 g��mol��1 |
| B��1 mol LiAlH4��125 ����ȫ�ֽ⣬ת��3 mol���� |
| C��LiAlH4��������ˮ����ɫ��Һ����ѧ����ʽ�ɱ�ʾΪLiAlH4��2H2O=LiAlO2��4H2�� |
| D��LiAlH4����ȩ���������Ҵ���LiAlH4����ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ѧ����ʽ�а�����˳��ļ������ǣ�8��2��5��1��4��1��5 |
| B����Ӧ������������N2O |
| C����Ӧ������ת�Ƶĵ�����Ϊ8mol���� |
| D����������ͻ�ԭ��������ʵ���֮��Ϊ4��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ��� | ��Ӧ�� | ���� |
| �� | KMnO4��H2O2��H2SO4 | K2SO4��MnSO4�� |
| �� | Cl2��FeBr2 | FeCl3��FeBr3 |
| �� | MnO4-�� | Cl2��Mn2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
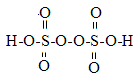
| A��CuO | B��MnO2 | C��Fe2O3 | D��NaNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������Ӧ�Ƿ��ȷ�Ӧ |
| B��������ɫ������ԭ�������ɵ�P2O5��ɫ����С�������̣���ˮ�Ժ�ǿ�����տ����е�ˮ�֣���������СҺ�Σ����� |
| C���÷�Ӧ�������뻹ԭ�����ʵ���֮��Ϊ6:5 |
| D��������Ӧ������3molPʱ��ת�Ƶ��ӵ����ʵ���Ϊ15mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��PbO2Ϊ��ԭ�������л�ԭ�� |
| B�����������뻹ԭ��������ʵ���֮��Ϊ5:2 |
| C������1 mol��Pb2+��ת�Ƶĵ�����Ϊ 5 mol |
| D�����Ի�����PbO2 ��������ǿ�ڵ�MnO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��MnO4-��H+����������Fe2+�ǻ�ԭ�� |
| B��H2O���������������ǻ�ԭ���� |
| C��ÿ����1molˮ��ת��1.2 mol�ĵ��� |
| D��Fe2+�Ļ�ԭ��ǿ��Mn2+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com