
一定温度下2L的密闭容器中发生反应:2X(g)+3Y(g)⇌2Z(g),测得X、Y、Z的浓度分别为0.2mol/L、0.3mol/L、0.4mol/L,再经过10分钟时反应达到平衡状态,下列结论不正确的是( )
|
| A. | 若起始时加入容器的只有反应物X、Y,则起始加入的X、Y的物质的量之比一定是2:3 |
|
| B. | 若起始时加入容器的有X、Y、Z,则起始时加入的X、Y的物质的量之比一定是2:3,而Z的物质的量一定小于1.2mol |
|
| C. | 达到平衡状态时,Z的浓度可能是0.1mol/L也可能是0.6mol/L |
|
| D. | 达到平衡状态时,X的浓度可能是0.1mol/L也可能是0.4moL/L |
| 化学平衡的影响因素;化学平衡建立的过程. | |
| 专题: | 化学平衡专题. |
| 分析: | 可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物不可能100%地全部转化为生成物;化学平衡的建立,既可以从正反应开始,也可以从逆反应开始,或者从正逆反应开始,不论从哪个方向开始,物质都不能完全反应,利用极限法假设完全反应,全部转到一边,求算各物质浓度的取值范围,据此判断分析. |
| 解答: | 解:若反应向正反应进行到达平衡,X2、Y2的浓度最小,Z的浓度最大,假定完全反应,则: 2X(g)+3Y(g)⇌2Z(g) 开始(mol/L) 0.2 0.3 0.4 变化(mol/L) 0.2 0.3 0.2 平衡(mol/L) 0 0 0.6 若反应向逆反应进行到达平衡,X2、Y2的浓度最大,Z的浓度最小,假定完全反应,则: 2X(g)+3Y(g)⇌2Z(g) 开始(mol/L) 0.2 0.3 0.4 变化(mol/L):0.4 0.6 0.4 平衡(mol/L):0.6 0.9 0 由于为可能反应,物质不能完全转化所以平衡时浓度范围为:0<c(X)<0.6,0<c(Y)<0.9,0<c(Z)<0.6, A、若起始时加入容器的只有反应物X、Y,则n(X)=0.6mol,n(Y)=0.9mol,其物质的量之比为2:3,故A正确; B、若起始时加入容器的只有反应物Z,n(Z)=1.2mol,起始时加入容器的有X、Y、Z,且X、Y的物质的量之比为2:3,所以则起始时加入的X、Y的物质的量之比一定是2:3,而Z的物质的量一定小于1.2mol,故B正确; C、Z的范围为0<c(Z)<0.6,所以达到平衡状态时,Z的浓度可能是0.1mol/L也可能是0.6mol/L,故C正确; D、X的范围为0<c(X)<0.6,所以说达到平衡状态时,X的浓度可能是0.1mol/L也可能是0.4moL/L是错误的,故D错误; 故选D. |
| 点评: | 本题考查了化学平衡的建立,难度不大,关键是利用可逆反应的不完全性,运用极限假设法解答,假设法是解化学习题的常用方法. |


科目:高中化学 来源: 题型:
我国稀土资源丰富,下列有关稀土元素14462Sm与15062Sm的说法正确的是 ( )
A.14462Sm与15062Sm互为同位素
B.14462Sm与15062Sm的质量数相同
C.14462Sm与15062Sm是同一种核素
D.14462Sm与15062Sm的核外电子数和中子数均为62
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中的杂质(括号内为杂质),所用试剂和方法正确的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 溴乙烷(乙醇) | 乙酸、浓硫酸 | 蒸馏 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| D | 甲烷(丙烯) | 溴水 | 洗气 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于太阳能、生物质能、氢能的说法不正确的是( )
|
| A. | 太阳能是地球上最基本的能源,绿色植物通过光合作用将太阳能转化成化学能 |
|
| B. | 农业上的秸秆、枝叶、水生植物、动物粪便及城市和工业的有机废弃物(如废弃塑料、橡胶等)都蕴藏着丰富的生物质能 |
|
| C. | 生物质能的利用主要有直接燃烧、生物化学转化、热化学转化等形式 |
|
| D. | 氢能是理想的清洁能源,但氢气的获取、贮存、运输等一直阻碍着人们大量利用氢能的步伐;贮氢合金的发现和利用,开辟了解决氢气贮存、运输难题的新途径 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化规律不属于元素性质周期性变化规律的是( )
|
| A. | 第二周期N、O、F单质的沸点依次升高 |
|
| B. | 第三周期的P、S、Cl的氢化物的稳定性依次增强 |
|
| C. | 第三周期的P、S、Cl的最高价含氧酸的酸性依次增强 |
|
| D. | 第三周期的Na、Mg、Al的最高价氧化物的水化物的碱性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
元素A和B的原子序数都小于18.已知A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a﹣2b),L层电子数为(a+b),则A、B两元素所形成的化合物的性质可能有( )
|
| A. | 能与水反应 | B. | 能与氢氧化钠溶液反应 |
|
| C. | 能与硫酸反应 | D. | 能与碳酸钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与人类生产、生活密切相关,下列有关说法不正确的是
A.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
B.福尔马林可浸制标本,利用了其使蛋白质变性的性质
C.医用酒精是用淀粉类植物发酵经蒸馏制成,浓度通常是75%
D.绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。
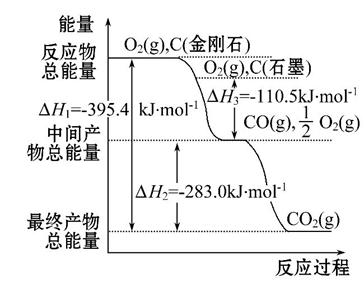
(1)等质量的金刚石和石墨完全燃烧 (填“金刚石”或“石墨”)放出
热量更多,写出表示石墨燃烧热的热化学方程式 。
(2)在通常状况下,金刚石和石墨相比 (填“金刚石”或“石墨”)更稳定,写出石墨转化为金刚石的热化学方程式 。
(3)12 g石墨在一定量空气中燃烧,生成气体36 g,该过程放出的热量为
。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于某些离子的检验及结论一定正确的是( )
|
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32﹣ |
|
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42﹣ |
|
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
|
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com