
 .
. ,C的最高价氧化物的水化物化学式为:Al(OH)3.
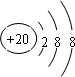
,C的最高价氧化物的水化物化学式为:Al(OH)3.分析 A元素原子的K层和M层电子数相同,说明原子核外有3个电子层,最外侧电子数为2,应为Mg,B元素原子的L层比K层电子数多5个,原子核外各层电子分别为2、7,应为F元素,C元素的+3价阳离子和氖原子具有相同的电子数,应为Al元素,D元素的原子核外有4个电子层,K层与L层电子数之和等于M层与N层电子数之和,说明原子核外各层电子数分别为2、8、8、2,应为Ca元素,结合题目分析解答.
解答 解:A元素原子的K层和M层电子数相同,说明原子核外有3个电子层,最外侧电子数为2,应为Mg,B元素原子的L层比K层电子数多5个,原子核外各层电子分别为2、7,应为F元素,C元素的+3价阳离子和氖原子具有相同的电子数,应为Al元素,D元素的原子核外有4个电子层,K层与L层电子数之和等于M层与N层电子数之和,说明原子核外各层电子数分别为2、8、8、2,应为Ca元素,
①通过以上分析知,A为Mg,故答案为:Mg;
②C为Al元素,C的阳离子电子式为:Al3+,D是Ca元素,溶液中D元素的结构示意图为 ,
,
故答案为:Al3+; ;
;
③D的最高价氧化物的水化物是氢氧化钙,氢氧化钙的电子式为 ,C的最高价氧化物的水化物是Al(OH)3,
,C的最高价氧化物的水化物是Al(OH)3,
故答案为: ;Al(OH)3;
;Al(OH)3;
④B是F元素,其氢化物的结构式为H-F,
故答案为:H-;
⑤熔融状态下氯化铝不导电,所以工业上采用电解熔融氧化铝的方法冶炼Al,反应方程式为2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑,
故答案为:氯化铝为共价化合物,熔化时不导电;2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑.
点评 本题考查原子结构和元素周期律的关系,为高频考点,侧重考查学生分析判断及知识综合应用能力,明确元素周期表结构及原子结构、元素化合物性质是解本题关键,知道工业上不能用电解氯化铝冶炼Al的原因,为易错点.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 只能有一种分类标准 | B. | 分类标准不同,物质所属类别不同 | ||
| C. | 可能有多种分类标准 | D. | 一种分类标准对应一种分类结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 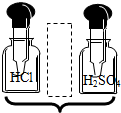 | B. | 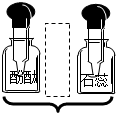 | C. |  | D. | 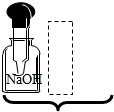 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、C1-、$SO_4^{2-}$、K+ | B. | H+、S2-、Na+、NO3- | ||
| C. | Ca2+、$HCO_3^-$、C1-、K+ | D. | Ag+、$NO_3^-$、Cl-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15mol/L | B. | 0.10mol/L | C. | 0.50mol/L | D. | 0.20mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
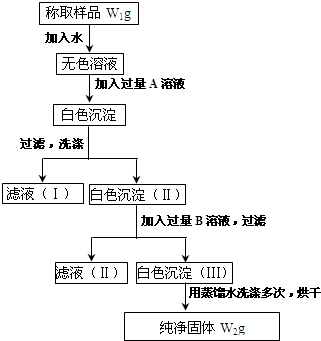
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com