
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口处 | |
| C. | 蒸发结晶时应将溶液完全蒸干 | |
| D. | 洗涤沉淀的方法是向漏斗中加水,使水没过沉淀,等水流完后再重复操作几次 |
分析 A.为了避免污染试剂,分液漏斗下层液体从下口放出,上层液体从上口倒出;
B.温度计用于测定馏分温度,需要放在蒸馏烧瓶的支管口处;
C.将溶液完全蒸干,会导致固体飞溅;
D.洗涤沉淀时,向过滤器中加入适量蒸馏水,然后让水自然流下.
解答 解:A.分液操作时,避免污染试剂,分液漏斗下层液体从下口放出,分液漏斗的上层液体从上口倒出,故A正确;
B.蒸馏操作时,用温度计测定馏分温度,便于控制馏分,应使温度计水银球靠近蒸馏烧瓶支管口处,故B正确;
C.蒸发结晶时,当出现大量晶体或剩余少量溶液时停止加热,利用余热蒸干即可,不能将溶液完全蒸干,故C错误;
D.沉淀的洗涤方法是:沿玻璃棒向过滤器中的沉淀上加蒸馏水至没过沉淀,让水自然流下,重复2~3次,故D正确;
故选C.
点评 本题考查了化学实验方案的评价,题目难度不大,明确常见化学实验基本操作方法即可解答,试题侧重基础知识的考查,有利于提高学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 移液时,不慎将液体流到瓶外 | |
| B. | 容量瓶中原有少量的蒸馏水 | |
| C. | 容量瓶盛过Na2CO3溶液,使用前未洗涤 | |
| D. | 定容时读数仰视 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积减半,则压强为原来的两倍 | |
| B. | 平衡向右移动,混合气体的颜色一定会变浅 | |
| C. | 平衡向右移动,混合气体的密度不变 | |
| D. | 体积减半,压强增大,但小于原来的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
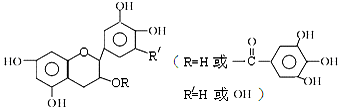
| A. | 儿茶素能与FeCl3溶液发生显色反应 | |
| B. | 1mol儿茶素最多可与10mol NaOH反应 | |
| C. | 常温下,儿茶素不溶于水,也不溶于有机溶剂 | |
| D. | 儿茶素一定不能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验Fe(NO3)2样品已被氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 |
| B | 提取碘水中碘 | 将碘水倒入分液漏斗,加入适量乙醇,振荡后静置 |
| C | 验证Mg(OH)2沉淀可以转化为 Fe(OH)3沉淀 | 向 2mL1mol•L-1NaOH 溶液中加入2~3 滴 lmol•L-1MgCl2溶液,生成白色沉淀,再加入2~3滴lmol•L-1FeCl3溶液 |
| D | 比较碳和硅的非金属性强弱 | 向饱和的Na2SiO3溶液中通人CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐可作调味剂,也可作食品防腐剂 | |
| B. | Na2O2和Na2O均可常用作呼吸面具中的供氧剂 | |
| C. | “熬胆矾铁釜,久之亦化为铜”,是因为熬制过程发生了置换反应 | |
| D. | 古剑“沈卢”“以剂钢为刃”柔铁为蒸干,不尔则多断折”,剂钢是指铁合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释时.在$\frac{c(O{H}^{-})}{C({H}^{+})}$的值增大的溶液中可大量存在:MnO4-、CO32-、K+、NH4+ | |
| B. | 100℃时,将pH=2的硫酸溶液与pH=12的氢氧化钠溶液等体积混合,溶液显中性 | |
| C. | 25℃时,NaB溶液的pH=9,则c(Na+ )-c(B-)=9.9×10-6mol•L-1 | |
| D. | 将0.2mol•L-1 的一元弱酸HA溶液和0.1mol•L-1 的NaOH溶液等体积混合:2c(OH-)+c(A-)=2c(H+)+c(HA) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com