
分析 电解质溶液导电性能力离子浓度成正比,离子浓度越大物质的水溶液导电性越强,单位体积的溶液中离子数目不变,导电性基本不变,据此分析解答.
解答 解:用溶质的质量分数为10%的盐酸做导电性实验,然后均匀通入氨气,随着氨气的通入,发生反应:NH3+H+═NH4+,反应前后单位体积的溶液中离子数目不变、离子电荷数也不变,所以溶液 导电性基本不变,
故答案为:基本不变,发生反应:NH3+H+═NH4+,单位体积的溶液中离子数目不变、离子电荷数也不变.
点评 本题主要考查电解质的概念、导电能力与离子浓度的关系,溶液的导电能力与溶液中的离子浓度和离子带电荷数有关,掌握基础是关键,题目较简单.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 28gCO和N2混合气体中含有原子总数为2NA | |
| B. | 在1L1mol•L-1的氨水中含有NA个NH3分子 | |
| C. | 标准状况下,11.2LNO和11.2LO2混合后气体分子数为NA | |
| D. | 1mol Fe分别与足量Cl2、S反应,Fe失去电子数都为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
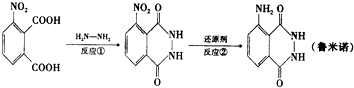
| A. | 1:2 | B. | 1:1 | C. | 2:1 | D. | 2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “84”消毒液可以与福尔马林溶液混合使用 | |
| B. | NaClO的稳定性和漂白性都比HClO强 | |
| C. | 工业上在特定条件下电解饱和食盐水制得NaClO,原理为:NaCl+H2O═NaClO+H2↑ | |
| D. | NaClO溶液在空气中发生离子反应为:2ClO-+CO2+H2O═2HClO+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
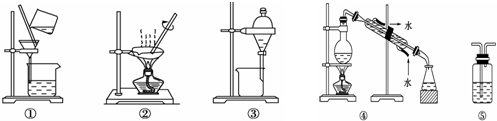
| A. | 分离Na2CO3溶液和苯,选④ | B. | 用CCl4提取碘水中的碘,选③ | ||
| C. | 用FeCl2溶液吸收Cl2,选⑤ | D. | 粗盐提纯,选①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜与盐酸反应:H++OH-═H2O | |
| B. | 铝粉与氢氧化钠溶液反应:Al+2OH-═AlO2-+H2↑ | |
| C. | 利用腐蚀法制作印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| D. | 在氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
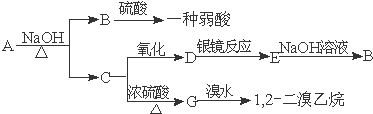
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com