
 3Fe+CO2的反应中,______是氧化剂,______是还原剂,______元素被氧化,______元素被还原.
3Fe+CO2的反应中,______是氧化剂,______是还原剂,______元素被氧化,______元素被还原. 3Fe+CO2的反应中,铁元素的化合价降低,则Fe3O4为氧化剂,Fe元素被还原,碳元素的化合价升高,则CO为还原剂,碳元素被氧化,
3Fe+CO2的反应中,铁元素的化合价降低,则Fe3O4为氧化剂,Fe元素被还原,碳元素的化合价升高,则CO为还原剂,碳元素被氧化, ,HCl参加反应生成盐时表现酸性,生成氯气时体现其还原性,即在该反应中HCl既有酸性又有还原性是②,
,HCl参加反应生成盐时表现酸性,生成氯气时体现其还原性,即在该反应中HCl既有酸性又有还原性是②,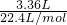 =0.15mol,由2KClO3+4HCl(浓)═2KCl+2ClO2↑+Cl2↑+2H2O可知,参加反应的KClO3物质的量为0.15mol×2=0.3mol,
=0.15mol,由2KClO3+4HCl(浓)═2KCl+2ClO2↑+Cl2↑+2H2O可知,参加反应的KClO3物质的量为0.15mol×2=0.3mol, ;②;0.3mol.
;②;0.3mol.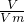 计算氯气的物质的量,根据反应方程式计算参加反应的KClO3物质的量.
计算氯气的物质的量,根据反应方程式计算参加反应的KClO3物质的量.

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省济宁市重点中学高一上学期期中考试化学试卷 题型:填空题
(10分)
(1)在Fe3O4 +4CO 3Fe+4CO2的反应中, 是氧化剂,
3Fe+4CO2的反应中, 是氧化剂,
是还原剂, 元素被氧化, 元素被还原。
(2)配平下列化学方程式并用单线桥法分析下列氧化还原反应中电子转移的方向和数目,
Cu + HNO3(浓) — Cu(NO3)2 + NO2↑ + H2O
浓硝酸表现出来的性质是_______________(填写编号)。
①还原性 ②酸性 ③氧化性
查看答案和解析>>
科目:高中化学 来源:2011-2012年黑龙江哈九中高一上学期期中考试化学试卷 题型:填空题
(10分)
1)在Fe3O4 +4CO 3Fe+4CO2的反应中,
是氧化剂,
是还原剂,
元素被氧化,
元素被还原。
3Fe+4CO2的反应中,
是氧化剂,
是还原剂,
元素被氧化,
元素被还原。
2)配平下列化学方程式并用单线桥法分析下列氧化还原反应中电子转移的方向和数目,
Cu + HNO3(浓) — Cu(NO3)2 + NO2↑ + H2O
浓硝酸表现出来的性质是_______________(填写编号)。?
①还原性 ②酸性 ③氧化性 ?
查看答案和解析>>
科目:高中化学 来源:2011-2012学年黑龙江省哈尔滨九中高一(上)期中化学试卷(解析版) 题型:填空题
 3Fe+4CO2的反应中, 是氧化剂, 是还原剂, 元素被氧化, 元素被还原.
3Fe+4CO2的反应中, 是氧化剂, 是还原剂, 元素被氧化, 元素被还原.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com