
【题目】I.部分弱酸的电离平衡常数如表:
弱酸 | HCOOH | HNO2 | H2S | H2SO3 | H2C2O4 | H2CO3 |
电离平衡常数(25℃) | K=1.8×10-4 | K=5.1×10-4 | K1=9.1×10-8 K2=1.1×10-12 | K1=1.23×10-2 K2=6.6×10-8 | K1=5.4×10-2 K2=5.4×10-5 | K1=4.3×10-7 K2=5.6×10-11 |
(1)上表的6种酸进行比较,酸性最弱的是:___;HCOO-、S2-、HSO3-3种离子中,最难结合H+的是___。
II.已知在室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,回答下列问题:
(1)两溶液中c(H+)·c(OH-)=___。
(2)各取5mL上述溶液,分别加水稀释至50mL,pH较大的是__溶液。
(3)各取5mL上述溶液,分别加热到90℃,pH较小的是___溶液。
(4)两溶液中由水电离出的c(H+)分别为:H2SO4溶液___;NH4Cl溶液__。
(5)取5mLNH4Cl溶液,加水稀释至50mL,c(H+)___10-6mol·L-1(填“>”、“<”或“=”),![]() __(填“增大”、“减小”或“不变”)
__(填“增大”、“减小”或“不变”)
【答案】H2S HSO3- 1×10-14 H2SO4 NH4Cl 1×10-9mol/L 1×10-5mol/L > 减小
【解析】
I. (1)上表的6种酸进行比较,酸性最弱的酸是电离平衡常数最小的酸,若为二元弱酸,主要看K1,比较表中数据,可得出酸性最弱的是H2S;HCOO-、S2-、HSO3-这3种离子中;对应酸电离平衡常数越大,电离产生的酸根离子结合H+的能力越弱,所以最难结合H+的是电离平衡常数最大的酸,分析表中数据,最难结合H+的是HSO3-。答案为:H2S;HSO3-;
II.(1)两溶液中c(H+)·c(OH-),等于室温时水的离子积常数1×10-14。答案为:1×10-14;
(2)加水稀释后H2SO4溶液中H+直接稀释,而NH4Cl溶液中NH4++H2O![]() NH3·H2O+H+平衡右移, H+的浓度减小得没有硫酸溶液中多,pH增大程度较小,故pH较大的是H2SO4溶液。答案为:H2SO4;
NH3·H2O+H+平衡右移, H+的浓度减小得没有硫酸溶液中多,pH增大程度较小,故pH较大的是H2SO4溶液。答案为:H2SO4;
(3)升高温度促进NH4+的水解,H+浓度增大,pH减小,而硫酸在水溶液中完全电离,H+浓度不变,故pH较小的是NH4Cl溶液。答案为:NH4Cl;
(4)由水电离的c(H+)等于由水电离出的c(OH-),故H2SO4溶液中,H+可认为完全由酸电离,因此水电离出的H+等于水电离出的c(OH-)=![]() =10-9 mol/L,NH4Cl溶液中的水电离出H+均来自于水的电离,因此水电离的c(H+)=1×10-5 mol/L。答案为:1×10-9mol/L;1×10-5mol/L;
=10-9 mol/L,NH4Cl溶液中的水电离出H+均来自于水的电离,因此水电离的c(H+)=1×10-5 mol/L。答案为:1×10-9mol/L;1×10-5mol/L;
(5)加水稀释后使平衡NH4++H2O![]() NH3·H2O+H+右移,故c(H+)>10-6mol/L,
NH3·H2O+H+右移,故c(H+)>10-6mol/L,![]() ,n(H+)增大,n(NH4+)减小,则
,n(H+)增大,n(NH4+)减小,则![]() 减小,。答案为:>;减小。
减小,。答案为:>;减小。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】硫代硫酸钠俗称保险粉,可用于照相业作定影剂、纸浆漂白作脱氯剂等。实验室用SO2通入Na2S和Na2CO3的混合溶液中来制备硫代硫酸钠。本实验对Na2S纯度要求较高,利用项图所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水。按下图所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热。待烧瓶中固体不再减少时,停止加热。将烧瓶取下,立即趁热过滤,再冷却结晶,过滤。将所得固体洗涤、干燥,得到Na2S9H2O晶体。

(1)下列说法不正确的是______。
A.将晶体转移至布氏漏斗时,若器壁上粘有少量晶体,应用冷水淋洗
B.抽滤时,为防止滤纸穿孔,可适当关小水龙头或多加一层滤纸
C.洗涤时,可用一定浓度的乙醇溶液洗涤晶体,目的是洗除晶体表面的杂质,易于得到干燥晶体
D.为加快产品的干燥,可高温烘干
E.在提纯过程中“趁热过滤”操作的目的是防止硫化钠结晶析岀而损失、去除杂质
(2)用下图所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是______,三颈烧瓶中发生反应的化学方程式______。

(3)保险粉样品中Na2S2O35H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为2Na2S2O3+I2=2NaI+Na2S4O6,准确称取Wg样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用0.1000mol/L碘的标准溶液进行滴定。请回答:
①到达滴定终点的标志______;
②滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为______,产品的纯度为______(设Na2S2O35H2O相对分子质量为M)。
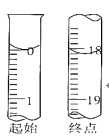
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O35H2O的纯度的测量结果______(“偏高”、“偏低”或“不变”)。
(4)某研究小组以硫代硫酸钠与硫酸反应来探究外界条件对反应速率的影响,设计实验如下:
实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
体积/mL | 浓度/mol/L | 体积/mL | 浓度/mol/L | |||
① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
下列有关说法不正确的是______。
A.该同学在实验中采用的研究方法是实验比较法
B.实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响
C. 实验①和③溶液变浑浊的时间相同
D.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和实验⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实:①NaHSO4溶液呈酸性;②长期使用化肥(NH4)2SO4会使土壤酸性增大,发生板结;③配制CuCl2溶液,用稀盐酸溶解CuCl2固体;④NaHS溶液中c(H2S)>c(S2-);⑤氯化铵溶液可去除金属制品表面的锈斑。其中与盐类的水解有关的叙述有( )
A.6项B.5项C.3项D.4项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是有关外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是( )
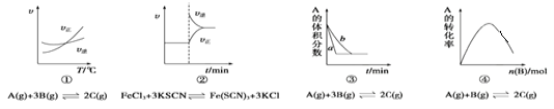
A.①是其他条件一定时,反应速率随温度变化的图像,则逆反应ΔH>0
B.②是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图像
C.③是在有无催化剂存在条件下,建立平衡过程的图像,a是使用催化剂时的曲线
D.④是一定条件下,向含有一定量A的恒容密闭容器中逐渐加入B,达平衡时A的转化率变化的图象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:CO(g)+Cl2(g)![]() COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法中正确的是
A. 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B. 该反应正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D. 若起始时向容器Ⅰ加入CO0.8mol、Cl20.8mol,达到平衡时CO转化率大于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
A. K=![]()
B. K=![]()
C. 增大c(H2O)或减小c(H2),会使该反应平衡常数减小
D. 改变反应的温度,平衡常数不一定变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料, 原料的综合利用率较高。其主要流程如下:
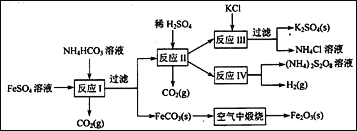
(1)反应I前需在FeSO4溶液中加入_____(填字母),以除去溶液中的Fe3+。
A.锌粉 | B.铁屑 | C.KI溶液 | D.H2 |
(2)反应I需控制反应温度低35℃,其目的是______________________。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是:________。
(4)反应Ⅳ常被用于电解生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极
发生的电极反应可表示为:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向20 mL 0.1 mol/L HA溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中不正确的是

A. 由题可知HA为弱酸
B. 滴定终点位于c和d之间
C. 滴定到b点时:n(Na+)+ n(H+)-n(OH-)+ n(HA)=0.002 mol
D. 滴定到d点时:c(OH-)>c(Na+)>c(A-) >c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近美国学者成功实现用氮气和水生产氨,其装置如下图所示:

下列说法正确的是
A. 上图中的能量转化方式只有2种
B. a极发生的电极反应为N2 + 6H+ + 6e- = 2NH3
C. 装置工作时H+ 向b极区移动,电解质溶液pH减小
D. a极区与b极区产生的气体的物质的量之比为1 :1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com