
下列情况能发生消去反应的是( )
A.1-溴丙烷与NaOH醇溶液共热
B.氯乙烷与NaOH的水溶液共热
C.乙醇与浓H2SO4共热至140℃
D.乙醇与浓H2SO4共热至170℃
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
下列关于胶体的说法中正确的是( )
A.溶液和胶体的本质区别是当一束光线通过胶体时可出现一条光亮的通路,溶液则没有此现象
B.制备Fe(OH)3胶体的方法是将饱和氯化铁溶液加热煮沸
C.静电除尘,利用了胶体电泳
D.胶体不均一、不稳定,静置易产生沉淀;溶液均一、稳定,静置不产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:
(1)海水提溴过程中,向浓缩的海水中通入________,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO ,其离子方程式为__________________________________________。
,其离子方程式为__________________________________________。
(2)溴与氯能以共价键结合形成BrCl。BrCl分子中,________显正电性。BrCl与水发生反应的化学方程式为____________________________________________。
(3)CuBr2分解的热化学方程式为:
2CuBr2(s)===2CuBr(s)+ Br2(g)
ΔH=+105.4 kJ/mol
在密闭容器中将过量CuBr2于487 K下加热分解,平衡时p(Br2)为4.66×103 Pa。
①如反应体系的体积不变,提高反应温度,则p(Br2)将会________(填“增大”“不变”或“减小”)。
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式不正确的是( )
A.醋酸溶液中加入少量氢氧化镁固体:Mg(OH)2+2CH3COOH===Mg2++2CH3COO-+2H2O
B.H2O2溶液中加入足量酸性KMnO4溶液:2MnO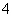 +3H2O2+6H+===2Mn2++6H2O+4O2↑
+3H2O2+6H+===2Mn2++6H2O+4O2↑
C.Ca(HCO3)2溶液中加入足量澄清石灰水:Ca2++HCO +OH-===CaCO3↓+H2O
+OH-===CaCO3↓+H2O
D.NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO 恰好沉淀完全:NH
恰好沉淀完全:NH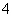 +H++SO
+H++SO +Ba2++2OH-===NH3·H2O+BaSO4↓+H2O
+Ba2++2OH-===NH3·H2O+BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
“乙醇汽油”就是在汽油里加入适量的乙醇混合而成的一种燃料。下列有关叙述不正确的是( )
A.汽车使用乙醇汽油能减少有害气体的排放
B.工业上常用裂化的方法提高汽油的产量和质量
C.乙醇汽油是多种烃的混合物
D.用玉米、高粱发酵可以制得乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应的实质是“旧键的断裂和新键的形成”。在一定条件下,一个乙醇分子断键只失去两个氢原子,生成的新有机化合物可能有(写结构简式,不一定填满)_______________;__________;______________;________________。根据你学习过的知识和提供的试剂、仪器,实现上述某一种转化,并验证该转化后的有机化合物。试剂:无水乙醇、光亮的铜丝、氢氧化钠溶液、硫酸铜溶液。仪器:试管、试管夹、镊子、胶头滴管、酒精灯、火柴。
(1)乙醇的转化:
①实验方案是_____________________________________;
②实验现象是_____________________________________;
③乙醇转化的化学方程式________________________。
(2)产物的验证:
①决定该有机化合物的主要性质的原子团的结构式是________,名称是______________。
②已知结构相似的物质,具有相似的化学性质。试用这一原理验证由乙醇转化成的有机物:首先配制试剂(写试剂名称)__________ _,然后将该试剂与被验证的有机化合物混合,并加热至沸腾,观察到的现象是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
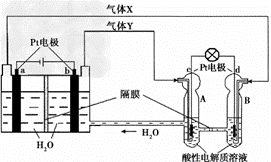
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池。右图为RFC工作原理示意图,有关说法正确的是
A.当有0.1 mol电子转移时,a极产生 0.56 L O2(标准状况下)
B.左端装置中化学能转化为电能,右端装置中电能转化为化学能
C.d极上发生的电极反应是:O2 + 4H+ + 4e- 2H2O
D.c极上进行还原反应,右端装置B中的H+可以通过隔膜进入A
查看答案和解析>>
科目:高中化学 来源: 题型:
铁是地壳中含量第二的金属元素,其单质、合金及化合物在生产生活中的应用广泛。
(一)工业废水中含有一定量的Cr2O72−和CrO42−,它们会对人类及生态系统产生很大的危害,必须进行处理。常用的处理方法是电解法,该法用Fe作电极电解含Cr2O72−的酸性废水,随着电解的进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(1)用Fe作电极的目的是_______________________________。
(2)阴极附近溶液pH升高的原因是_______________________________(用电极反应式解释);溶液中同时生成的沉淀还有________________。
(二)氮化铁磁粉是一种磁记录材料,利用氨气在400℃以上分解得到的氮原子渗透到高纯铁粉中可制备氮化铁。制备高纯铁粉涉及的主要生产流程如下:
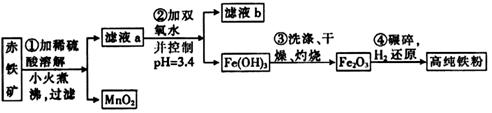
已知:①某赤铁矿石含60.0%Fe2O3、3.6%FeO,还含有Al2O3、MnO2、CuO等。
②部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 |
(3)步骤②中加双氧水的目的是_________________________,pH控制在3.4的作用是_____________________________;已知25℃时,Ksp[Cu(OH)2]=2.0×10-20,该温度下反应:Cu2++2H2O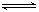 Cu(OH)2+2H+的平衡常数K=_______________。
Cu(OH)2+2H+的平衡常数K=_______________。
(4)制备氮化铁的反应:Fe+NH3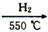 FexNy+H2(未配平),若整个过程中消耗氨气34.0g,消耗赤铁矿石2kg,设整个过程中无损耗,则FexNy磁粉的化学式为___________。
FexNy+H2(未配平),若整个过程中消耗氨气34.0g,消耗赤铁矿石2kg,设整个过程中无损耗,则FexNy磁粉的化学式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案中,不能达到实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
| D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com