
 某温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下,能够大量共存的一组离子是( )
某温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下,能够大量共存的一组离子是( )| A. | a点对应的溶液:Na+、K+、SO42-、Cl- | |
| B. | b点对应的溶液:I-、Mg2+、K+、ClO- | |
| C. | c点对应的溶液:Na+、S2-、F-、NH4+ | |
| D. | a点对应的溶液:CO32-、Cl-、Al3+、SO42- |
分析 A.a点c(H+)=c(OH-),溶液显中性;
B.b点c(H+)<c(OH-),溶液显碱性;
C.c点c(H+)>c(OH-),溶液显酸性;
D.a点c(H+)=c(OH-),溶液显中性,离子之间相互促进水解.
解答 解:A.a点c(H+)=c(OH-),溶液显中性,该组离子之间不反应,可大量共存,故A正确;
B.b点c(H+)<c(OH-),溶液显碱性,不能大量存在Mg2+,故B错误;
C.c点c(H+)>c(OH-),溶液显酸性,不能大量存在S2-、F-,故C错误;
D.a点c(H+)=c(OH-),溶液显中性,CO32-、Al3+相互促进水解生成沉淀和气体,不能共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、水解反应的判断,题目难度不大.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | W一定是氢元素 | |
| B. | 简单离子半径rz>rx>ry | |
| C. | 标准状况下,1mol Z的最高价氧化物的体积约为22.4L | |
| D. | 工业上常用电解熔融Y的氯化物的方法制备Y单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
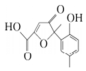
| A. | 该化合物分子中不含手性碳原子 | |
| B. | 该化合物与NaHCO3溶液作用有CO2气体放出 | |
| C. | 1 mol该化合物与足量溴水反应,消耗2 mol Br2 | |
| D. | 在一定条件下,该化合物与HCHO能发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 西维因分子式为C12H10NO2 | |
| B. | 西维因分子中至少有21个原子共平面 | |
| C. | 1mol西维因最多能与6mol氢气发生加成反应 | |
| D. | 取一段时间后的混合液,先用盐酸酸化,再滴加FeCl3溶液,可检验西维因是否发生水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由X与W形成的化合物是离子化合物 | |
| B. | Z元素的最低化合价为-1,最高化合价为+7 | |
| C. | Y的最高价氧化物对应水化物的酸性比U的强 | |
| D. | Z的简单离子半径小于U的简单阳离子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 重大节日期间燃放的焰火的颜色是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 小苏打是制作馒头和面包等糕点的膨松剂,也是治疗胃酸过多的一种药剂 | |
| C. | 为防止月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 | |
| D. | 大力实施矿物燃料的脱硫脱硝技术,可以减少SO2、NO2的排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有还原性,可用于漂白纸浆 | |
| B. | 碳酸氢钠能与碱反应,可用作食品的膨松剂 | |
| C. | 四氯化碳密度比水大,可用于萃取溴水中的Br2 | |
| D. | MgO、Al2O3的熔点都很高,都可用作耐火材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某科研单位利用电化学原理用SO2来制备硫酸,装置如图,含有某种催
某科研单位利用电化学原理用SO2来制备硫酸,装置如图,含有某种催查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com