
分析 在氢氧化铁胶体中加入硫酸,发生胶体的聚沉,先产生红褐色沉淀,氢氧化铁具有碱性,和硫酸发生中和反应,后沉淀溶解,胶体不能透过半透膜,用半透膜把制作的氢氧化铁胶体中含有的NaCl分离出来,为胶体的提纯,据此分析解答.
解答 解:胶体遇电解质溶液能发生聚沉,在氢氧化铁胶体中加入硫酸,发生胶体的聚沉,先产生红褐色沉淀,现象选③,氢氧化铁具有碱性,和硫酸发生中和反应,后沉淀溶解,
现象选②,性质为中和反应,选⑧,胶体不能透过半透膜,而溶液可以,将胶体和溶液用半透膜分离的方法叫渗析,所以用半透膜把制作的氢氧化铁胶体中含有的NaCl分离出来,选①,
故答案为:③②⑧①.
点评 本题考查胶体的性质,题目难度不大,注意胶体聚沉性质和氢氧化铁碱性的掌握.


 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 中子数为10的氧原子:${\;}_{10}^{18}$O | B. | 羟基的电子式: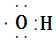 | ||
| C. | Na2S的电子式: | D. | CO2的结构式:O-C-O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应(1)和(2)均为氧化还原反应 | |
| B. | 反应(1)的氧化剂是O2,还原剂是FeO•Cr2O3 | |
| C. | 高温下,O2的氧化性大于Fe2O3小于Na2CrO4 | |
| D. | 生成1mol的Na2Cr2O7时共转移5mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 金属 | Ti | Mg | Cu |
| 金属表面现象 | 放出气泡速度缓慢 | 放出气泡速度快 | 无变化 |
| A. | 在地壳中的含量Mg>Ti,说明金属在地壳中的含量越低,活泼性越弱 | |
| B. | 反应中产生H2速李不同的原因是因为c(H+)不同 | |
| C. | 用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径 | |
| D. | 利用电解装置,Cu可以与稀硫酸反应产生H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 酸 | 电离常数 |
| 碳酸 | K1=4×10-7 K2=5.6×10-11 |
| 亚硫酸 | K1=1.54×10-2 K2=1.02×10-7 |
| A. | SO2+H2O+2CO32-=2HCO3-+SO32- | B. | SO2+2HCO3-=2CO2+SO32-+H2O | ||
| C. | 2SO2+H2O+CO32-=CO2+2HSO3- | D. | SO2+H2O+CO32-=HCO3-+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 已知图一表示的是可逆反应A(g)+B(g)?C(s)+D(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)?N2O4(g)△H<0的浓度(c)随时间t的变化情况.下列说法中正确的是( )
已知图一表示的是可逆反应A(g)+B(g)?C(s)+D(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)?N2O4(g)△H<0的浓度(c)随时间t的变化情况.下列说法中正确的是( )| A. | 若图一t2时改变的条件是增大压强,则反应的△H增大 | |
| B. | 图一t2时改变的条件可能是升高了温度或增大了压强 | |
| C. | 图二t1时改变的条件可能是升高了温度或增大了压强 | |
| D. | 若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol NaBH4与足量水反应(NaBH4+H2O→NaBO2+H2↑,未配平)时转移的电子数为8NA | |
| B. | 1 L 0.1mol•L-1NaF溶液中含有0.1NA个F- | |
| C. | 常温常压下,1mol NaHCO3与足量稀硫酸反应,生成气体的体积大于22.4L | |
| D. | 在标准状况下,22.4L氢气与22.4L氦气所含有的原子数均为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 转移时有溶液洒落在外 | B. | 定容时观察液面俯视 | ||
| C. | 有少量NaOH溶液残留在烧杯里 | D. | 容量瓶中原来有少量蒸馏水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com