
【题目】汽车尾气污染已成为突出的环境问题之一,反应![]()
![]() 可用于净化汽车尾气,已知该反应的反应速率极慢,
可用于净化汽车尾气,已知该反应的反应速率极慢,![]() 时平衡常数为
时平衡常数为![]() 。下列说法正确的是( )
。下列说法正确的是( )
A.提高尾气净化效率的最佳途径是研制高效催化剂
B.提高尾气净化效率的常用方法是降低温度
C.装有该尾气净化装置的汽车排出的气体中不再含有NO和CO
D.570K时及时抽走![]() 和
和![]() ,可使平衡正向移动,同时化学平衡常数将增大,尾气净化效率更佳
,可使平衡正向移动,同时化学平衡常数将增大,尾气净化效率更佳
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O是一种氧气吸收剂,为红棕色晶体,易被氧化,不溶于水和乙醚(易挥发的有机溶剂),微溶于乙醇,易溶于盐酸,其制备装置如下(已知Cr3+水溶液颜色为绿色,Cr2+水溶液颜色为蓝色):

(1)装置甲中连通管a的作用是________________________。
(2)向三颈烧瓶中依次加入过量锌粒、适量CrCl3溶液:关闭k2打开k1,旋开分液漏斗的旋塞并控制好滴速;当观察到三颈烧瓶中溶液颜色__________________时,打开k2关闭k1,当观察到装置乙中出现大量红棕色晶体时,关闭分液漏斗的旋塞。
(3)装置乙中反应的离子方程式为__________________________________。
(4)将装置乙中混合物快速过滤、洗涤和干燥,称量得到a g [Cr(CH3COO)2]2·2H2O。洗涤时依次用去氧的冷蒸馏水、无水乙醇、乙醚洗涤。其中乙醇洗涤的目的是___________。
(5)若实验所取用的CrCl3溶液中含溶质b g,则[Cr(CH3COO)2]2·2H2O (相对分子质量为376) 的产率是________________。
(6)该实验装置有一个明显的缺陷,解决此缺陷的措施为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫单质和化合物在工农业生产中有着重要的应用,而SO2直接排放会对环境造成危害。
Ⅰ.已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=+571.2 kJ·mol-1
BaS(s)=Ba(s)+S(s) ΔH=+460 kJ·mol-1
已知:2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s) ΔH=____________。
Ⅱ.SO2的尾气处理通常有以下几种方法:
(1)活性炭还原法:反应原理:恒温恒容时2C(s)+2SO2(g)![]() S2(g)+2CO2(g)。反应进行到不同时间测得各物质的浓度如图:
S2(g)+2CO2(g)。反应进行到不同时间测得各物质的浓度如图:
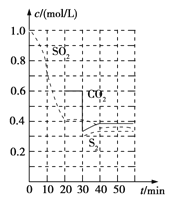
①0~20 min反应速率表示为v(SO2)=____________;
②30 min时,改变某一条件平衡发生移动,则改变的条件最有可能是____________;
③平衡常数的表达式K=____________。
(2)亚硫酸钠吸收法
①Na2SO3溶液吸收SO2的离子方程式为__________________;
②常温下,当吸收至NaHSO3时,吸收液中相关离子浓度关系一定正确的是____________(填序号)。
a.c(Na+)+c(H+)>c(SO32-)+c(HSO3-)+c(OH-)
b.c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3)
c.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)
d.水电离出c(H+)=1×10-8mol/L
(3)电化学处理法

①如图所示,Pt(Ⅰ)电极的反应式为__________________;
②当电路中转移0.02 mol e-时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加________mol离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3.5%(质量分数)CaO。
(1) Ca元素在周期表中位置是____,其原子结构示意图____。
(2) Ca与最活跃的非金属元素A形成化合物D,D的电子式为____,D的沸点比A与Si形成的化合物E的沸点____。
(3)配平用钙线氧脱鳞的化学方程式____:P+FeO+CaO![]() Ca3(PO4)2+Fe。
Ca3(PO4)2+Fe。
(4)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则金属M为______;检测Mn+的方法是_____(用离子方程式表达)。
(5)取1.6 g钙线试样,与水充分反应,生成224 mL H2(标准状况),再向溶液中通入适量的CO2,最多能得到CaCO3____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:![]()
![]()
![]() 在密闭容器反应,达到平衡状态的标志是( )
在密闭容器反应,达到平衡状态的标志是( )
(1)单位时间内生成n mol O2的同时生成2n mol NO2
(2)单位时间内生成n mol O2的同时生成2n mol NO
(3)用NO2、NO、O2的物质的量浓度变化表示反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的平均相对分子质量不再改变的状态
A.(1)(2)(3)(4)(5)B.(2)(3)(4)C.(1)(3)(4)(5)D.(1)(4)(5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为![]() 的密闭容器中反应
的密闭容器中反应![]()
![]() 达到平衡,下列说法正确的是
达到平衡,下列说法正确的是
容器 | 温度 | 物质的起始浓度 | ||
|
|
| ||
Ⅰ | 400 |
|
| 0 |
Ⅱ | 400 |
|
|
|
Ⅲ | 300 | 0 | 0 | td style="width:88.2pt; border-top-style:solid; border-top-width:0.75pt; border-left-style:solid; border-left-width:0.75pt; padding:3.38pt 5.03pt; vertical-align:middle">|
A.达到平衡时,向容器Ⅰ中通入氦气,正、逆反应速率均增大,平衡不移动
B.达到平衡时,容器Ⅱ中![]() 比容器Ⅰ中的大
比容器Ⅰ中的大
C.达到平衡时,容器Ⅲ中![]() 小于容器Ⅰ中
小于容器Ⅰ中![]() 的两倍
的两倍
D.容器中混合气体的密度不再发生变化可作为反应达到平衡状态的标志
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于可逆反应X(g)+3Y(g) ![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol·L-1、0.3mol·L-1、0.08mol·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol·L-1、0.3mol·L-1、0.08mol·L-1,则下列判断正确的是( )
A.c1∶c2=3∶1
B.平衡时,Y和Z的生成速率之比为2∶3
C.X、Y的转化率不相等
D.c1的取值范围为0mol·L-1<c1<0.14mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 电子云图中的小黑点密表示该核外空间的电子多
B. 电子排布式 1s22s22px2违反了洪特规则
C. 原子序数为7、8、9的三种元素,其第一电离能和电负性均依次增大
D. 元素周期表中Fe处于ds区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京航空航天大学教授偶然中发现米虫吃塑料,受此启发进行了系列实验,证实黄粉虫的肠道微生物可降解聚苯乙烯(PS),蜡虫可降解聚乙烯(PE)。聚苯乙烯在虫肠内降解的示意图如下,下列说法正确的是
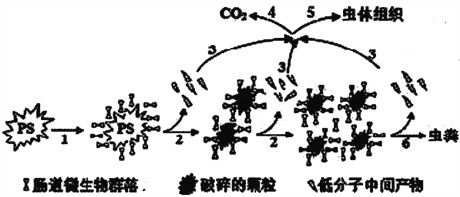
A. 在虫肠内微生物作用下,聚苯乙烯断裂碳碳双键
B. 在虫肠内微生物作用下,聚苯乙烯直接降解为CO2分子
C. 在虫肠内微生物作用下,聚苯乙烯发生降解,分子量降低
D. 聚乙烯与聚苯乙烯是同系物,具有烯烃的性质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com