
| A.Ca2+、H+、Cl-、HCO3- | B.Mg2+、Al3+、Cl-、SO42- |
| C.Na+、H+、NO3-、OH- | D.NH4+、Ag+、HCO3-、OH- |
科目:高中化学 来源:不详 题型:单选题
| A.pH=7的溶液中:Al3+、K+、SO42-、HCO3- |
| B.FeCl2溶液中:SO42-、H+、MnO4-、Na+ |
| C.能使pH试纸变深红色的溶液中:S2-、SO32-、S2O32-、SO42- |
| D.滴加甲基橙试剂显红色的溶液中:Na+、NH4+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al3+、K+、SO42-、NO3- | B.Na+、Mg2+、SO42-、Cl- |
| C.ClO-、I-、K+、Na+ | D.Ba2+、OH-、CO32-、K+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.盐溶液不是促进就是抑制水的电离 | B.弱酸对水的抑制作用就比强酸弱得多 |
| C.催化剂能改变可逆反应达到平衡的时间 | D.硫酸氢钠溶液显酸性,是因为电离大于水解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu2+、K+、SO42-、NO3- | B.NH4+、Ba2+、Cl―、HCO3- |
| C.Fe3+、Na+、NO3-、SCN- | D.K+、Na+、I-、NO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 。已知某澄清溶液常温下的AG=12,则在此溶液中能大量共存的离子组
。已知某澄清溶液常温下的AG=12,则在此溶液中能大量共存的离子组| A.Na+、AlO2-、K+、ClO- | B.MnO4-、K+、SO32-、Na+ |
| C.Mg2+、SO42-、HCO3-、Na+ | D.NH4+、NO3-、Al3+、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4+、Ba2+、SO42-、CL- | B.K+、Fe3+、CL-、OH- |
| C.K+、Na+、CO32-、SO42- | D.Na+、K+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
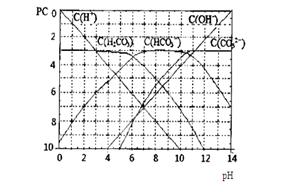
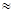
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
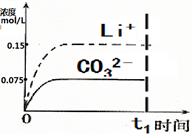
A.溶质的质量分数为w=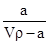 ×100% ×100% |
B.溶质的物质的量浓度c=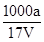 mol/L mol/L |
C.溶液中c(OH-)=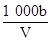 mol/L mol/L |
| D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com