
分析 ①同一周期,元素的金属性随着原子序数增大而减弱,同一主族元素,元素的金属性随着原子序数增大而增强,则在元素周期表中金属性最强的元素位于周期表左下角;
②地壳中含量最丰富的元素为O元素,主族元素原子核外电子层数与其周期数相同,最外层电子数与其族序数相同;
在11~17号的元素中;
③同一周期元素,原子半径随着原子序数增大而减小;同一周期元素,离子半径先减小后增大再减小;
④最高价氧化物中既能与盐酸,又能与烧碱反应的是两性氧化物.
解答 解:①同一周期,元素的金属性随着原子序数增大而减弱,同一主族元素,元素的金属性随着原子序数增大而增强,则在元素周期表中金属性最强的元素位于周期表左下角,在短周期中金属性最强的元素是Na,故答案为:Na;
②地壳中含量最丰富的元素为O元素,主族元素原子核外电子层数与其周期数相同,最外层电子数与其族序数相同,O原子核外有2个电子层、最外层有6个电子,则O元素位于第二周期第VIA族,
故答案为:二;VIA;
在11~17号的元素中;
③同一周期元素,原子半径随着原子序数增大而减小;同一周期元素,离子半径先减小后增大再减小,
则第三周期中原子半径最小的是Cl元素,阳离子半径最小的是Al 3+、阴离子半径最小的是Cl-,
故答案为:Cl;Al 3+;Cl-;
④最高价氧化物中既能与盐酸,又能与烧碱反应的是两性氧化物,第三周期中两性氧化物是Al2O3,
故答案为:Al2O3.
点评 本题考查元素周期表、元素周期律的综合运用,为高频考点,明确原子结构、元素周期表结构、元素周期律是解本题关键,侧重考查学生判断及知识综合运用能力,知道离子半径比较方法,注意基础知识的积累.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-542.7kJ/mol | |
| B. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1059.3kJ/mol | |
| C. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1076.7kJ/mol | |
| D. | N2H4(g)+$\frac{1}{2}$N2O4(g)=$\frac{3}{2}$N2(g)+2H2O(g)△H=-1076.7kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
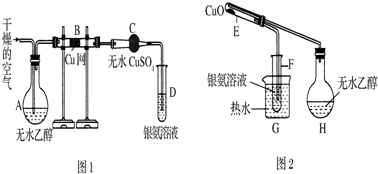
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3分子是非极性分子 | |
| B. | 分子内3个N-H键的键长不相等,键角不相等 | |
| C. | NH3分子内3个N-H键的键长相等,3个键角都等于107°18′ | |
| D. | NH3分子内3个N-H键的键长相等,3个键角都等于120° |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸、氢氧化钠、干冰 | B. | 澄清石灰水、铜、氨气 | ||
| C. | 石油、水、硫酸钡 | D. | 海水、氯化钠、氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有阴离子的化合物中一定含有阳离子 | |
| B. | 非金属元素组成的化合物一定是共价化合物 | |
| C. | 干冰升华时,分子内共价键会发生断裂 | |
| D. | 两种元素组成的分子中一定只有极性键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com