
【题目】根据所学知识,完成下列各题:
(1)在标准状况下,气体A的密度为3.17gL﹣1 , 则气体A的摩尔质量为;
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入某种物质M的饱和溶液,继续煮沸可制得一种红褐色胶体. ①物质M的名称为 .
②下列关于M的水溶液和上述操作所得胶体的叙述,正确的是
A.M的水溶液是电中性的,所得胶体是带电的
B.二者分散质的粒子都不能透过半透膜
C.二者可用丁达尔效应区别
D.向两者中逐滴滴加盐酸溶液均无明显现象
若胶体中含有杂质M则可用法提纯此分散系.
(3)同温同压下,同体积的CO2和CO,它们的分子数之比为 , 物质的量之比为 , 密度之比为 .
(4)V L硫酸铝溶液中含有m gAl3+ , 则溶液中SO42﹣的物质的量浓度是molL﹣1 , 硫酸铝的物质的量浓度是molL﹣1
(5)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g.此混合物中CO和CO2的物质的量比是 , CO的体积分数是 , C和O的原子个数比是 .
(6)3.01×1023个OH﹣的质量为 , 含有电子的物质的量为 , 和克Na+含有的离子数相同.
(7)欲除去粗盐中的Ca2+ , Mg2+ , SO42﹣等杂志,溶解后可依次加入、、 , 过滤出沉淀后再加入 , 蒸发结晶即可.(填写化学式)
【答案】
(1)71g/mol
(2)氯化铁;C;渗析
(3)1:1;1:1;11:7
(4)![]() ;
; ![]()
(5)1:3;25%;4:7
(6)8.5g;5mol;11.5
(7)BaCl2;NaOH;Na2CO3;HCl
【解析】解:(1)在标准状况下,气体A的密度为3.17gL﹣1,则气体A的摩尔质量M=ρVm=3.17gL﹣1×22.4L/mol=71g/mol,
所以答案是:71g/mol;(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入某种物质M的饱和溶液,继续煮沸可制得一种红褐色胶体,该胶体是氢氧化铁胶体,①实验室用氯化铁溶液制取氢氧化铁胶体,所以M名称是氯化铁,所以答案是:氯化铁;②A.M的水溶液是电中性的,胶体不导电,胶粒带电,故错误;
B.溶液能透过半透膜,胶体不能透过半透膜,故错误;
C.胶体具有丁达尔效应,溶液没有丁达尔效应,故正确;
D.将胶体中加入电解质溶液或产生聚沉现象,故错误;
故选C;
溶液能透过半透膜,胶体不能透过半透膜,所以若胶体中含有杂质M则可用渗析法提纯此分散系,
所以答案是:C;渗析;(3)同温同压下,气体摩尔体积相等,同体积的CO2和CO物质的量相等,物质的量之比为1:1,它们的分子数之比等于物质的量之比=1:1,密度之比等于摩尔质量之比=44g/mol:28g/mol=11:7,
所以答案是:1:1;1:1;7;(4)V L硫酸铝溶液中含有mg Al3+,铝离子的物质的量= ![]() =
= ![]() mol,c(Al3+)=
mol,c(Al3+)= ![]() =
= ![]() mol/L,该溶液中铝离子和硫酸根离子的物质的量浓度之比等于其系数之比=2:3,c(SO42﹣)=
mol/L,该溶液中铝离子和硫酸根离子的物质的量浓度之比等于其系数之比=2:3,c(SO42﹣)= ![]() c(Al3+)=
c(Al3+)= ![]() ×
× ![]() mol/L=
mol/L= ![]() mol/L;
mol/L;
根据原子守恒得c[Al2(SO4)3]= ![]() c(Al3+)=
c(Al3+)= ![]() ×
× ![]() mol/L=
mol/L= ![]() mol/L,
mol/L,
所以答案是: ![]() ;
; ![]() ;(5)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g,
;(5)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g,
设CO和CO2的物质的量分别是xmol、ymol
则 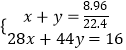
![]() ,
,
所以CO和CO2的物质的量之比=0.1mol:0.3mol=1:3;
根据V=nVm知,其体积之比等于物质的量之比,所以CO的体积分数等于其物质的量分数= ![]() =25%;
=25%;
该混合气体中C、O原子个数之比等于其物质的量之比=(0.1+0.3)mol:(0.1+0.3×2)mol=4:7,
所以答案是:1:3;25%;4:7;(6)3.01×1023个OH﹣的物质的量= ![]() =0.5mol,其质量m=nM=0.5mol×17g/mol=8.5g,每个氢氧根离子中含有10个电子,所以含有电子的物质的量为5mol;和Na+含有的离子数相同,说明二者物质的量相等,钠离子的质量m=nM=0.5mol×23g/mol=11.5g,
=0.5mol,其质量m=nM=0.5mol×17g/mol=8.5g,每个氢氧根离子中含有10个电子,所以含有电子的物质的量为5mol;和Na+含有的离子数相同,说明二者物质的量相等,钠离子的质量m=nM=0.5mol×23g/mol=11.5g,
所以答案是:8.5g;5mol;11.5;(7)欲除去粗盐中的Ca2+,Mg2+,SO42﹣等杂志,溶解后可依次加入氯化钡除去硫酸根离子、NaOH除去镁离子、碳酸钠除去钙离子和过量钡离子,最后过滤出沉淀后再加入稀盐酸,蒸发结晶即可,
所以答案是:BaCl2;NaOH;Na2CO3;HCl.
【考点精析】解答此题的关键在于理解胶体的重要性质的相关知识,掌握胶体的性质:①丁达尔现象(可用来鉴别胶体和溶液) ②布朗运动 ③电泳现象 ④胶体聚沉(加入电解质、加入带异种电荷的胶体、加热,均可使胶体聚沉).


科目:高中化学 来源: 题型:
【题目】I.根据所学知识,回答下列问题:
(1)元素周期表1~20号元素中,金属性最强的元素是______(填元素符号,下同);属于稀有气体的是_________;非金属性最强的元素在周期表中的位置是__________________。
(2)己知NO2和N2O4之间发生可逆反应:2NO2(g)(红棕色)![]() N2O4(g)(无色)。将装有NO2和N2O4混合气体的烧瓶浸入热水中,观察到的现象是_______,产生该现象的原因是________。
N2O4(g)(无色)。将装有NO2和N2O4混合气体的烧瓶浸入热水中,观察到的现象是_______,产生该现象的原因是________。
(3)一定条件下,向2L恒容密闭容器中按体积比1:3充入4.48L(标准状况)N2和H2的混合气体,发生反应N2(g)+3H2(g)![]() 2NH3(g),5min时反应达到平衡状态,测得c(N2)=0.02mol/L。
2NH3(g),5min时反应达到平衡状态,测得c(N2)=0.02mol/L。
①0~5min内,v(NH3)=_______________。
②下列叙述可证明上述反应达到平衡状态的是________(填序号)。
a.V(H2)=3v(N2)
b.容器内压强保持不变
c.每消耗ImolN2,同时生成2molNH3
d.N2、H2和NH3的物质的量浓度不再变化
II.五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C的简单离子和B的简单离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物中阴阳离子的个数比为1:1。回答下列问题:
(1)五种元素中,原子半径最大的是______(填元素名称),非金属性最强元素的是_________。
(2)由元素A分别和元素B、D、E所形成的共价型化合物中,热稳定性最差的是_____(用化学式表示)。
(3)元素A和E形成的化合物与元素A和B形成的化合物反应,产物的电子式为______,其中存在的化学键类型为______________。
(4)E离子的结构示意图是____________;元素D最高价氧化物的水化物的化学式为_____。
(5)单质E与水反应的离子方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2L甲气体和1L Y2气体恰好完全反应生成2L XY2气体(所有气体的体积在标准状况下测定)。则甲的分子式可能是( )
A.X2B.XYC.YX2D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某脂肪族化合物A的相对分子质量为118,其中C的质量分数为41%,H为5%,O为54%.化合物A能与碳酸氢钠溶液反应放出气体,也能与新制氧氧化铜悬浊液反应生成砖红色沉淀,符合条件的A的醇羟基同分异构体有( )
A.2种
B.3种
C.4种
D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,标准状况下某O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积应是( )
A.![]() L
L
B.![]()
C.![]()
D.![]() L
L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,1.7g氨气所占的体积为 L,它与标准状况下 L硫化氢含有相同数目的氢原子.
(2)某气态氧化物的化学式为RO2 , 在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为 ,R的相对原子质量为 .
(3)已知CO、CO2的混合气体质量共16.0g,标准状况下体积为8.96L,则可推知该混合气体中含CO g,所含CO2在标准状况下的体积为 L.
(4)同温同压下,SO2与氦气的密度之比为 ;若质量相同,两种气体的体积比为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A.标准状况下,18gD2O中所含的质子数为10NA
B.标准状况下,11.2LO2参加反应转移的电子数一定为2NA
C.28gN2和CO的混合气体中含有的分子数为NA
D.5.6g铁与足量稀硫酸反应失去电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装置Ⅰ、Ⅱ、Ⅲ是常用的三种制备气体的装置。装置B、C、D、E、G、H是用于制取氯气并进行漂白性质验证的装置。请根据装置和所给的试剂回答下列问题:


实验室提供的药品有:铜片、高锰酸钾、 二氧化锰、熟石灰、浓盐酸、过氧化氢、稀硝酸、浓硝酸、氯化铵。
(1)根据提供药品和装置Ⅰ、Ⅱ、Ⅲ完成下列有关问题:
①实验室制备氧气,可选用的装置是_________(填序号)。实验室制氨气所选试为__________。
②实验室制备NO气体的离子方程式为_____________________收集NO气体可采用的方法是______________法。
③检验Ⅲ装置气密性的过程是___________________________________________。
(2)现用提供的制备装置和装置B、C、D、E、G、H来完成实验室制备纯净氯气并进行氯气性质的验证实验。
①常温下,高锰酸钾和浓盐酸可以发生反应生成Cl2和可溶性MnCl2,该反应氧化剂的化学式为________________,氧化产物的化学式为_________________,反应的离子方程式为___________________________________。
②制备纯净氯气并验证能起漂白作用的是次氯酸而不是氯气,从左到右仪器的连接顺序为a→d→e→_____________________________________________________→f。
③装置D中发生反应的离子方程式为______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com