
某学生用碱式滴定管量取0.1mol·L-1的NaOH溶液,开始时仰视液面读数为1.00mL,取出部分溶液后,俯视液面,读数为11.00mL,该同学在操作中实际取出的液体体积为
A.大于10.00mL B.小于10.00mL C.等于10.00mL D.11.00mL
 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:填空题
研究大气中含硫化合物(主要是SO2和H2S)的转化具有重要意义。
(1)高湿条件下,写出大气中SO2转化为HSO3-的方程式:__________;____________。
(2)土壤中的微生物可将大气中H2S经两步反应氧化成SO42-,两步反应的能量变化示意图如下:
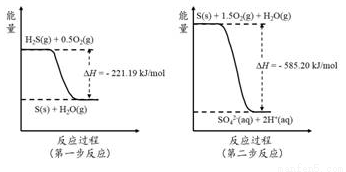
1mol H2S(g)全部氧化成SO42-(aq)的热化学方程式为_________________________。
(3)二氧化硫—空气质子交换膜燃料电池可以利用大气所含SO2快速启动,其装置示意图如下:
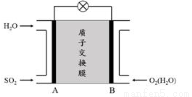
①质子的流动方向为_________________(“从A到B”或“从B到A”)。
②负极的电极反应式为__________________________。
(4)燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。SO2烟气脱除的一种工业流程如下:
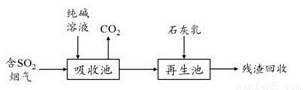
① 用纯碱溶液吸收SO2将其转化为HSO3-,反应的离子方程式是________________。
② 若石灰乳过量,将其产物再排回吸收池,其中可用于吸收SO2的物质的化学式是_____________。
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
下列与碳、氮、氧、硫、硅等非金属元素及其化合物有关的说法不正确的是
A.工业上,用焦炭在电炉中还原二氧化硅得到含杂质的粗硅
B.氮的氧化物是形成光化学烟雾的主要物质
C.NO2、CO2和SO2溶于水均可导电,它们都是电解质
D.将SO2通入酸化的Ba(NO3)2溶液中会出现白色沉淀
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:选择题
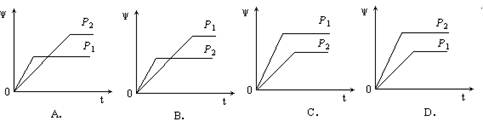
在一定温度不同压强 (p1<p2)下,可能反应2X(g)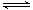 2Y(g)+Z(g)中, 生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
2Y(g)+Z(g)中, 生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:选择题
下列水溶液一定呈中性的是
A.c(NH4+)=c(C1-)的NH4Cl 溶液
B.c(H+)=1×10-7mol·L-1的溶液
C.pH=7的溶液
D.室温下将pH=3的酸与pH= 11的碱等体积混合后的溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海省高二11月月考化学试卷(解析版) 题型:选择题
以下是表示反应2A+B=3C+4D的反应速率数据。按照反应快慢顺序排列应为( )[
①υ(A)=0.5mol·L-1·S-1 ②υ(B)=0.3mol·L-1·S-1
③υ(C )=0.8mol·L-1·S-1 ④υ(
)=0.8mol·L-1·S-1 ④υ( D)=1mol·L-1·S-1
D)=1mol·L-1·S-1
A.④>③>①>② B.②>③>①=④ C.②>③>①>④ D.③>②>①=④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海省高二11月月考化学试卷(解析版) 题型:选择题
25℃、101 kPa下,1g氢气燃烧生成液态水,放出142.9kJ热量,能表示H2燃烧热的热化学方程式为( )
A.2H2(g)+O2(g) = 2H2O(1) △H=―571.6kJ/mol
B.2H2(g)+O2(g) = 2H2O(1) △H=+571.6 kJ/mol
C.H2(g)+ O2(g) = H2O(g) △H=―285.8 kJ/mol
O2(g) = H2O(g) △H=―285.8 kJ/mol
D.H2(g)+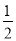 O2(g) = H2O(1) △H=―285.8kJ/mol
O2(g) = H2O(1) △H=―285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一期中化学卷(解析版) 题型:选择题
下列反应中Cl元素全部被氧化的是
A.KClO3+6HCl=KCl+3Cl2↑+3H2O
B.2NaCl电解2Na+Cl2↑
C.H2+Cl2光照2HCl
D.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2 O
O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二11月月考化学试卷(解析版) 题型:实验题
NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有:Cu、Zn、Fe、Cr等杂质)为原料获得。工艺流程如下图:
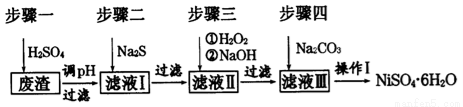
请回答下列问题:
(1)用稀硫酸溶解废渣时,为了提高浸取速率可采取的措施有_____________(任写一点)。
(2)向滤液中滴入适量的Na2S溶液,目的是除去Cu2+、Zn2+,写出除去Cu2+的离子方程式:_______________。
(3)上述流程中滤液Ⅲ的主要成分是___________。
(4)确定步骤四中Na2CO3溶液足量,碳酸镍己完全沉淀的简单实验方法是______________。
(5)操作I的实验步骤依次为(实验中可选用的试剂:溶液、蒸馏水、pH试纸):
①_______________;
②_______________;
③蒸发浓缩、冷却结晶,过滤得NiSO4·6H2O晶体
④ 用少量乙醇洗涤NiSO4·6H2O晶体并晾干
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com