
| A. | 电负性:As>Cl>P | B. | 热稳定性:HCl>HBr>AsH3 | ||
| C. | 第一电离能:Br>Se>As | D. | 酸性:H3AsO4>H2SO4>H3PO4 |
分析 A.非金属性越强,电负性越大;
B.元素的非金属性越强,其气氢化物的热稳定性越强;
C、As处于VA,外围电子处于半满的较稳定结构,故As的第一电离能大于Se;
D、非金属性越强,最高价氧化物的水化物酸性越强.
解答 解:A.非金属性为Cl>P>As,则电负性为Cl>P>As,故A错误;
B.元素的非金属性越强,其气氢化物的热稳定性越强,非金属性:Cl>Br>As,所以稳定性HCl>HBr>AsH3,故B正确;
C.As处于VA,外围电子处于半满的较稳定结构,故As的第一电离能大于Se,所以第一电离能:Br>Se>As,故C错误;
D、非金属性S>P>As,最高价氧化物的水化物酸性为H2SO4>H3PO4>H3AsO4,故D错误;
故选B.
点评 本题考查非金属性的性质,为高频考点,把握元素的位置、性质及元素周期律等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:实验题
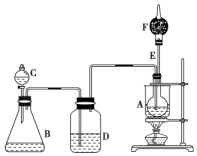 已知CH3CH2OH+NaBr+H2SO4CH3CH2Br+NaHSO4+H2O,如图是某校化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图.
已知CH3CH2OH+NaBr+H2SO4CH3CH2Br+NaHSO4+H2O,如图是某校化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体一定是均一、透明、介稳的 | B. | 用丁达尔效应区别胶体和溶液 | ||
| C. | 可以用滤纸来分离胶体和溶液 | D. | 胶体只能在液体中形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在有机物分子中碳原子所连的4个原子或原子团均不相同时,该碳原子叫手性碳原子,含有手性碳原子的有机物具有光学活性,下边有机物含有一个手性碳原子(*C表示手性碳原子),具有光学活性.若要消除其光学活性,可选用下列哪些化学反应( )
在有机物分子中碳原子所连的4个原子或原子团均不相同时,该碳原子叫手性碳原子,含有手性碳原子的有机物具有光学活性,下边有机物含有一个手性碳原子(*C表示手性碳原子),具有光学活性.若要消除其光学活性,可选用下列哪些化学反应( )| A. | 只有①②③ | B. | 只有④⑤⑥ | C. | 只有①②④⑤⑥ | D. | 以上都可以 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 再通入1molO2,平衡正向移动,平衡常数不变 | |
| B. | 降低温度,正反应速率先减小后增大 | |
| C. | 平衡时SO2气体的转化率为50% | |
| D. | 该条件下反应放出0.5QkJ的热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com