
分析 碱金属的化学性质按照Li、Na、K、Rb的顺序逐渐增强,碱金属和水反应产生氢气的物质的量和金属的物质的量是相等的,相同条件下,质量相等时,金属相对分子质量越小,则物质的量越大,据此分析.
解答 解:碱金属的活泼性按照Li、Na、K、Rb的顺序逐渐增强,所以三种金属各1g,分别与足量的水反应,最剧烈的是铷;碱金属和水反应产生氢气的物质的量和金属的物质的量是相等的,相同条件下,质量相等时,金属相对分子质量越小,则物质的量越大,所以生成H2体积最大的是锂;
故答案为:铷;锂.
点评 本题考查了碱金属的性质,侧重于元素周期律的应用的考查,注意把握同主族金属元素性质的递变规律,题目难度不大.


科目:高中化学 来源: 题型:实验题
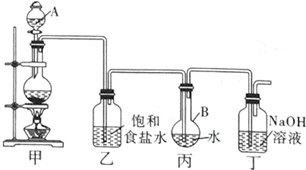
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
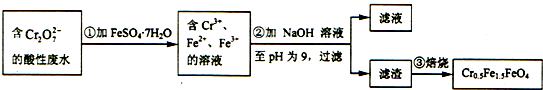
| A. | 根据第①步反应可知还原性:Cr3+大于Fe2+ | |
| B. | 第②步过滤得到的滤渣中主要成分为Cr(OH)3、Fe(OH)2,不含Fe(OH)3 | |
| C. | 欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4,理论上需要加入27.8g FeSO4•7H2O | |
| D. | 第③步高温焙烧过程用到的主要实验仪器中属于硅酸盐质的有:酒精灯、蒸发皿、泥三角 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 中和热是在稀溶液中,酸和碱反应生成1mol水所放出的热量.某同学利用50mL 0,.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和热测定的实验,回答下列问题:
中和热是在稀溶液中,酸和碱反应生成1mol水所放出的热量.某同学利用50mL 0,.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和热测定的实验,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
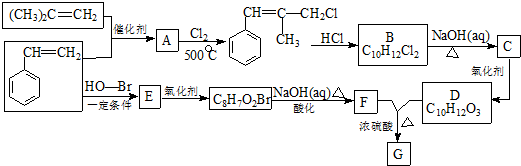
 .
.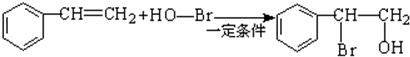 .
.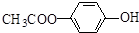 和
和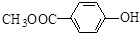 .
.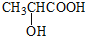 ) 的合成路线:
) 的合成路线: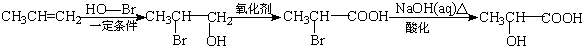 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
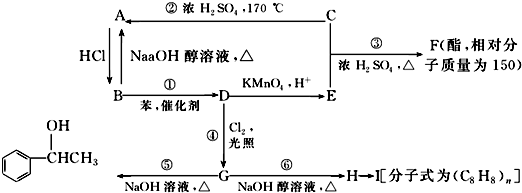
 .
. ;
; .
.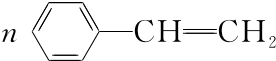 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$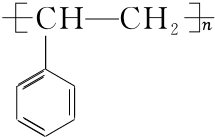 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com