
Cl2ŹĒ·ÄÖƹ¤ŅµÖŠ³£ÓƵÄĘÆ°×¼Į£¬Na2S2O3æÉ×÷ĪŖĘưײ¼Ę„ŗóµÄ”°ĶŃĀČ¼Į”±£®S2O32©ŗĶCl2·“Ó¦µÄ²śĪļÖ®Ņ»ĪŖSO42©£®ĻĀĮŠĖµ·ØÖŠ£¬²»ÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | øĆ·“Ó¦ÖŠŃõ»Æ¼ĮŹĒCl2 |
| ”” | B£® | øł¾ŻøĆ·“Ó¦æÉÅŠ¶Ļ»¹ŌŠŌ£ŗS2O32©£¾Cl© |
| ”” | C£® | ÉĻŹö·“Ó¦ÖŠ£¬ĆæÉś³É1 mol SO42©£¬æÉĶŃČ„2mol Cl2 |
| ”” | D£® | SO2ÓėĀČĘųµÄĘÆ°×ŌĄķĻąĶ¬£¬ĖłŅŌŅ²æÉŅŌÓĆSO2×ö·ÄÖƹ¤ŅµµÄĘÆ°×¼Į |
| Ńõ»Æ»¹Ō·“Ó¦£»Ńõ»Æ»¹Ō·“Ó¦µÄ¼ĘĖć£®. | |
| ×ØĢā£ŗ | Ńõ»Æ»¹Ō·“Ó¦×ØĢā£® |
| ·ÖĪö£ŗ | S2O32©ŗĶCl2·“Ó¦µÄ²śĪļÖ®Ņ»ĪŖSO42©£¬SŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬ŌņClŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬½įŗĻŃõ»Æ»¹Ō·“Ó¦ÖŠµÄøÅÄī¼°¹ęĀÉĄ“½ā“š£® |
| ½ā“š£ŗ | ½ā£ŗS2O32©ŗĶCl2·“Ó¦µÄ²śĪļÖ®Ņ»ĪŖSO42©£¬SŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬ŌņClŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ A£®ŅņClŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ĖłŅŌŃõ»Æ¼ĮŹĒCl2£¬¹ŹAÕżČ·£» B£®ÓÉ»¹Ō¼ĮµÄ»¹ŌŠŌ“óÓŚ»¹Ō²śĪļµÄ»¹ŌŠŌæÉÖŖ£¬»¹ŌŠŌ£ŗS2O32©£¾Cl©£¬¹ŹBÕżČ·£» C£®ĆæÉś³Él mol SO42©£¬Óɵē×ÓŹŲŗćæÉÖŖ£¬×ŖŅĘ4molµē×Ó£¬ŌņæÉĶŃČ„2mol Cl2£¬¹ŹCÕżČ·£» D£®SO2ÓėĀČĘųµÄĘÆ°×ŌĄķ²»ĻąĶ¬£¬ĀČĘųŹĒĄūÓĆĘäŃõ»ÆŠŌ£¬¶ų¶žŃõ»ÆĮņŹĒĄūÓĆ»ÆŗĻ·“Ó¦£¬¹ŹD“ķĪó£» ¹ŹŃ”D£® |
| µćĘĄ£ŗ | ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦£¬Ć÷Č·Ļ°ĢāÖŠµÄŠÅĻ¢ŹĒ½ā“šµÄ¹Ų¼ü£¬×„×”S2O32©ŗĶCl2·“Ó¦µÄ²śĪļÖ®Ņ»ĪŖSO42©¼“æɽā“š£¬×¢Ņāµē×ÓŹŲŗćµÄÓ¦ÓĆ£¬ĢāÄæÄѶČÖŠµČ£® |


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷×éĄė×Ó£¬ŌŚČÜŅŗÖŠÄÜ“óĮæ¹²“ę”¢¼ÓČėNaOHČÜŅŗŗó¼ÓČČ¼ČÓŠĘųĢå·Å³öÓÖÓŠ³ĮµķÉś³ÉµÄŅ»×éŹĒ ( ””””)
””””)
A£®Ba2£«”¢NO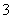 ”¢NH
”¢NH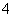 ”¢Cl£
”¢Cl£
B£®Ca2£«”¢HCO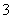 ”¢NH
ӢNH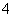 ӢAlO
ӢAlO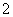
C£®K£«”¢Ba2£«”¢Cl£”¢HSO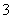
D£®Mg2£«”¢NH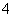 ”¢SO
”¢SO ”¢K£«
”¢K£«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
“×ĖįŹĒŅ»ÖÖ³£¼ūµÄČõĖį£¬ĪŖĮĖÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ£¬Ä³Ķ¬Ń§æŖÕ¹ĮĖĢāĪŖ”°“×ĖįŹĒČõµē½āÖŹµÄŹµŃéĢ½¾æ”±µÄĢ½¾æ»ī¶Æ”£øĆĶ¬Ń§Éč¼ĘĮĖČēĻĀ·½°ø£¬ĘäÖŠ“ķĪóµÄŹĒ(””””)
A£®ĻČÅäÖĘŅ»¶ØĮæµÄ0.10 mol/L CH3COOHČÜŅŗ£¬Č»ŗó²āČÜŅŗµÄpH£¬ČōpH“óÓŚ1£¬ŌņæÉÖ¤Ć÷“×ĖįĪŖČõµē½āÖŹ
B£®ĻČÅäÖĘŅ»¶ØĮæ0.01 mol/LŗĶ0.10 mol/L µÄCH3COOHČÜŅŗ£¬·Ö±šÓĆpH¼Ę²āĖüĆĒµÄpH£¬ČōĮ½ÕßµÄpHĻą²īŠ”ÓŚ1øöµ„Ī»£¬ŌņæÉÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ
C£®ĻČ²ā0.10 mol/L CH3COOHČÜŅŗµÄpH£¬Č»ŗó½«Ęä¼ÓČČÖĮ100”ę£¬ŌŁ²āpH£¬Čē¹ūpH±äŠ”£¬ŌņæÉÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ
D£®ÅäÖĘŅ»¶ØĮæµÄCH3COONaČÜŅŗ£¬²āĘäpH£¬Čō³£ĪĀĻĀpH“óÓŚ7£¬ŌņæÉÖ¤Ć÷“×ĖįŹĒČõµē½āÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | ±ź×¼×“æöĻĀ£¬11.2 LŅŅĻ©ŗ¬ÓŠµÄ¼«ŠŌ¹²¼Ū¼üŹżĪŖNA |
| ”” | B£® | ³£ĪĀĻĀ£¬5.6 L NOŗĶ5.6 L O2µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.5NA |
| ”” | C£® | 16.9 g BaO2¹ĢĢåÖŠŅõ”¢ŃōĄė×Ó×ÜŹżĪŖ0.2NA |
| ”” | D£® | ŗ¬ÓŠ1 mol Fe£ØOH£©3µÄĒāŃõ»ÆĢś½ŗĢåÖŠŗ¬ÓŠ½ŗĮ£ŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | NaHSO4”¢Na2O2¾§ĢåÖŠµÄŅõ”¢ŃōĄė×ÓøöŹż±Č¾łĪŖ1£ŗ2 |
| ”” | B£® | Ąė×Ó»ÆŗĻĪļÖŠŅ»¶Ø²»ŗ¬¹²¼Ū¼ü |
| ”” | C£® | ijÖ÷×åŌŖĖŲµÄ×īøß¼Ūŗ¬ŃõĖįĪŖHnROm£¬ŌņĘäĘųĢ¬Ēā»ÆĪļŅ»°ćŹĒH2m©nR |
| ”” | D£® | ŌŖĖŲÖÜĘŚ±ķÖŠL²ćµē×ÓĪŖĘꏿµÄŌŖĖŲĖłŌŚ×åŠņŹżÓėøĆŌŖĖŲŌ×ÓµÄL²ćµē×ÓŹżĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠĖÄÖÖČ¼ĮĻµē³Ų£ŗA£®¹ĢĢåŃõ»ÆĪļČ¼ĮĻµē³Ų£¬B£®¼īŠŌĒāŃõ»ÆĪļČ¼ĮĻµē³Ų£¬C£®ÖŹ×Ó½»»»Ä¤Č¼ĮĻµē³Ų£¬D£®ČŪČŚŃĪČ¼ĮĻµē³Ų£¬ĻĀĆęŹĒ¹¤×÷ŌĄķŹ¾ŅāĶ¼£¬ĘäÖŠÕż¼«·“Ӧɜ³ÉĖ®µÄŹĒ£Ø””””£©
| ”” | A£® |
| B£® |
| C£® |
| D£® |
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
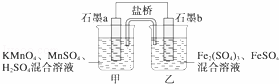
Ä³ŃŠ¾æŠŌѧĻ°Š”×éøł¾Ż·“Ó¦2KMnO4+10FeSO4+8H2SO4ØT2MnSO4+5Fe2£ØSO4£©3+K2SO4+8H2OÉč¼ĘČēĶ¼Ōµē³Ų£¬ĘäÖŠ¼×”¢ŅŅĮ½ÉÕ±ÖŠø÷ĪļÖŹµÄĪļÖŹµÄĮæÅØ¶Č¾łĪŖ1mol•L©1£¬ČÜŅŗµÄĢå»ż¾łĪŖ200mL£¬ŃĪĒÅ֊װӊ±„ŗĶK2SO4ČÜŅŗ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©“ĖŌµē³ŲµÄÕż¼«ŹĒŹÆÄ«””””£ØĢī”°a”±»ņ”°b”±£©£¬·¢Éś””””·“Ó¦£®
£Ø2£©µē³Ų¹¤×÷Ź±£¬ŃĪĒÅÖŠµÄSO42©ŅĘĻņ””””£ØĢī”°¼×”±»ņ”°ŅŅ”±£©ÉÕ±£®
£Ø3£©Į½ÉÕ±ÖŠµÄµē¼«·“Ó¦Ź½·Ö±šĪŖ
¼×””””£¬
ŅŅ””””£®
£Ø4£©Čō²»æ¼ĀĒČÜŅŗµÄĢå»ż±ä»Æ£¬MnSO4ÅØ¶Č±äĪŖ1.5mol•L©1£¬Ōņ·“Ó¦ÖŠ×ŖŅʵĵē×ÓĪŖ””””mol£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠÓŠ¹Ųµē½āÖŹČÜŅŗÖŠĪ¢Į£µÄĪļÖŹµÄĮæÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | pH=3µÄŅ»ŌŖĖįŗĶpH=11µÄŅ»ŌŖĒæ¼īµČĢå»ż»ģŗĻŗóµÄČÜŅŗÖŠ£ŗc£ØOH©£©=c£ØH+£© |
| ”” | B£® | ŌŚ0.1 mol•L©1Na2CO3ČÜŅŗÖŠ£ŗc£ØOH©£©©c£ØH+£©=c£ØHCO3©£©+2c£ØH2CO3£© |
| ”” | C£® | ŅŃÖŖµžµŖĖį£ØHN3£©Óė“×ĖįĖįŠŌĻą½ü£¬ŌņŌŚNaN3Ė®ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”Ė³ŠņĪŖ£ŗc£ØNa+£©£¾c£ØOH¯£©£¾c£ØN3¯£©£¾c£ØH+£© |
| ”” | D£® | 0.2 mol•L©1NaHCO3ČÜŅŗÖŠ¼ÓČėµČĢå»ż0.1 mol•L©1NaOHČÜŅŗ£ŗc£ØCO32©£©£¾c£ØHCO3©£©£¾c£ØOH©£©£¾c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĪļÖŹÖŠÄܵ¼µē£¬µ«ÓÖ²»ŹĒµē½āÖŹŗĶ·Ēµē½āÖŹµÄ“æ¾»ĪļŹĒ(””””)
A£®ČŪČŚµÄNaCl B£®ŹÆÄ«¾§Ģå
C£®ŅŗĀČ D£®ŃĪĖį
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com