
分析 根据氯原子守恒计算x的值,根据A原子守恒计算A的物质的量,再根据M=$\frac{m}{n}$计算A的摩尔质量.
解答 解:根据氯原子守恒,有0.800mol×x=1.2mol×2,解得x=3,
根据A原子守恒可知,n(A)=n(AClx)=0.800mol,故M(A)=$\frac{21.6g}{0.800mol}$=27g/mol,所以A是铝,反应方程式为:2Al+3Cl2=2AlCl3,
故答案为:(1)2Al+3Cl2=2AlCl3;(2)3;(3)27g/mol.
点评 本题考查质量守恒定律的有关计算,然后结合相对分子质量确定元素的种类,书写化学方程,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④ | C. | ③④ | D. | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某人的血糖检测结果为90mg/dL,他的血糖是正常(人的血糖正常值在3.61----6.11mmol/L,血糖相对分子质量180) | |
| B. | 用点燃的火柴在液化气钢瓶口检验是否漏气 | |
| C. | 当光束通过有尘埃的空气、氯化铁溶液、墨水等分散系能观察到丁达尔现象 | |
| D. | 胶体属于介稳体系原因是胶体带电 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
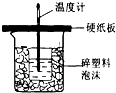 中和热是指酸跟碱发生中和反应生成lmolH2O所放出的热量.某学生想通过测反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
中和热是指酸跟碱发生中和反应生成lmolH2O所放出的热量.某学生想通过测反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20Ne和22Ne互为同位素 | B. | 20Ne和22Ne的电子数不同 | ||
| C. | 20Ne和22Ne的质量数相同 | D. | 20Ne和22Ne的中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 84% | B. | 60% | C. | 91% | D. | 42% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol任何物质都含有约6.02×1023个原子 | |
| B. | 0.012 kg 12C中约含有6.02×1023个碳原子 | |
| C. | 1 mol水中含有2 molH和1 molO | |
| D. | 1 mol氦气含有6.02×1023个原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com