
【题目】在一定温度下,反应A2(g)+B2(g)![]() 2AB(g)达到限度的标志是( )
2AB(g)达到限度的标志是( )
A. 单位时间内生成n mol A2同时生成n mol AB
B. 容器内的总物质的量不随时间变化
C. 单位时间内生成2n mol AB的同时生成n mol B2
D. 单位时间内生成n mol A2的同时生成n mol B2
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列们关说法正确的是
A. 石墨具有良好的润滑性,故可用做电池的电极材料。
B. 碳酸钠溶液呈碱性,故可用带玻璃塞的试剂瓶盛放
C. 液氮的沸点较低,故可为超导材料提供低温环境
D. 单晶硅的硬度较高,故可用于制备电子芯片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
A.短周期元素形成离子后,最外层都达到8电子稳定结构
B.第二周期元素的最高正化合价等于它所处的主族序数
C.同一元素可能既表现金属性,又表现非金属性
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子中不同的化学键如图,关于乙醇在各种反应中断裂键的说法不正确的是( )
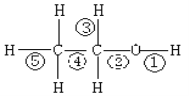
A. 乙醇和钠反应,键①断裂
B. 在铜催化下和O2反应,键①③断裂
C. 1700C乙醇制乙烯时,键②⑤断裂
D. 1400C乙醇制乙醚的反应,键①⑤断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的叙述中不正确的是( )
A.第ⅡA族中无非金属元素
B.0族中无金属元素
C.第ⅠA族元素单质均能与水反应生成H2
D.金属元素的种类比非金属元素多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列各组微粒或物质:
A.O2和O3 B.![]() C和
C和![]() C
C
C.CH3CH2CH2CH3和CH3CH2CH(CH3)CH3
D.CH3CH2CH2CH3和CH(CH3)3
(1)________组两种微粒互为同位素。
(2)_______组两种物质互为同素异形体。
(3)________组两种物质属于同系物。
(4)_______组两物质互为同分异构体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(![]() ),其原理如下图所示,下列说法正确的是
),其原理如下图所示,下列说法正确的是

A. 该装置为电解装置,B为阳极
B. 电子是从A极沿导线经小灯泡流向B极
C. A极的电极反应式为![]()
D. 当外电路中有0.1mole-转移时,A极区增加的H+的个数为0.05NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( ) 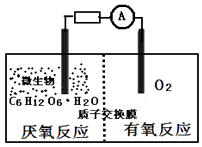
A.负极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从正极区移向负极区
D.电池总反应为C6H12O6+6O2═6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性碳催化下合成.
(1)实验室中常用来制备氯气的化学方程式为;
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(△H)分别为﹣890.3kJmol﹣1、﹣285.8 kJmol﹣1和﹣283.0 kJmol﹣1 , 则生成1 m3(标准状况)CO所需热量为;
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,其反应的化学方程式为;
(4)COCl2的分解反应为COCl2(g)═Cl2(g)+CO(g)△H=+108 kJmol﹣1 . 反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出): 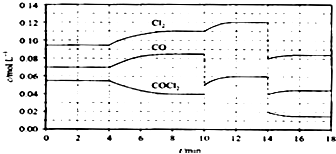
①计算反应在第8min时的平衡常数K=;
②比较第2min反应温度T(2)与第8min反应温度T(8)的高低:T(2) T(8)(填“<”、“>”或“=”);
③若12min时反应于温度T(8)下重新达到平衡,则此时c(COCl2)=molL﹣1
④比较产物CO在2﹣3min、5﹣6min和12﹣13min时平均反应速率[平均反应速率分别以v(2﹣3)、v(5﹣6)、v(12﹣13)表示]的大小;
⑤比较反应物COCl2在5﹣6min和15﹣16min时平均反应速率的大小:v(5﹣6) v(15﹣16)(填“<”、“>”或“=”),原因是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com