
【题目】有关物质的转化关系如下图所示(部分物质与条件已略去)。A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物;I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中。

请回答下列问题:
(1) H的化学式为________________。
(2) D的电子式为________________。
(3) 写出反应①的化学方程式:________________。
(4) 写出G的水溶液与C的硝酸盐溶液反应的离子方程式:________________。
【答案】 Al2O3 ![]() 3Fe+4H2O(g)
3Fe+4H2O(g)![]() Fe3O4+4H2 Al3++3NH3·H2O===Al(OH)3↓+3NH
Fe3O4+4H2 Al3++3NH3·H2O===Al(OH)3↓+3NH![]() (或Al3++3NH3+3H2O===Al(OH)3↓+3NH
(或Al3++3NH3+3H2O===Al(OH)3↓+3NH![]() )
)
【解析】A是最常见的无色液体,应为H2O,F是一种具有磁性的化合物,应为Fe3O4,由转化关系可知B为Fe,E为H2,D在空气中的含量最多,应为N2,则G为NH3,H是既能与强酸反应又能与强碱反应的氧化物,H为Al2O3,F和C在高温下反应,则C为Al;I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中,应为AlN。
(1)由以上分析可知H为Al2O3,故答案为:Al2O3;
(2)D为N2,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)铁和水反应生成四氧化三铁和氢气,方程式为3Fe+4H2O(g)![]() Fe3O4+4H2,故答案为:3Fe+4H2O(g)
Fe3O4+4H2,故答案为:3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
(4)氨水呈碱性,和硝酸铝反应生成氢氧化铝,离子方程式为Al3++3NH3H2O=Al(OH)3↓+3NH4+,故答案为:Al3++3NH3H2O=Al(OH)3↓+3NH4+。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是( )
A.制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3↓+3H+
B.H2SO4溶液中投入锌粒:2H++Zn═H2↑+Zn2+
C.用NaHCO3 治疗胃酸过多:HCO3﹣+H+═CO2↑+H2O
D.氯化铁和氢氧化钾溶液混合:Fe3++3OH﹣═Fe(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)=3C(g)+4D(g)反应中,表示该反应速率最快的数据是( )
A. vA=0.5 mol /(L·s) B. vB=0.3 mol/(L·s)
C. vC=0.8 mol /(L·s) D. vD=1 mol /(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上或实验室提纯以下物质的方法不合理的是(括号内为杂质)( )
A.溴苯(溴):加NaOH溶液,分液
B.乙烷(乙烯):通入溴水,洗气
C.乙酸(水):加新制生石灰,蒸馏
D.乙酸乙酯(乙酸):加饱和碳酸钠溶液,分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科学与材料、人体健康和环境保护等密切相关。
(1) 材料是人类社会发展的重要物质基础。
①高炉炼铁和生产硅酸盐水泥都要用到的原料是________(填字母)。
a. 黏土 b. 石灰石 c. 焦炭
②铝合金制品用途广泛。下列有关铝合金的性质正确的是________(填字母)。
a. 耐腐蚀 b. 强度小 c. 密度大
③玻璃钢具有质轻、电绝缘性好、强度大等特点。玻璃钢属于________(填字母)。
a. 金属材料 b. 无机非金属材料 c. 复合材料
(2) 合理饮食和正确用药,是人体健康的重要保证。现有下列五种物质A. 食盐 B. 小苏打 C. 苹果汁 D. 葡萄糖 E. 青霉素,
请按下列要求填空(填序号)。
富含维生素C的是____________;可直接进入血液,补充能量的是________;应用最广泛的抗生素之一的是________;既可作为疏松剂,又可治疗胃酸过多的是________;食用过多会引起血压升高、肾脏受损的是________。
(3) 治理环境污染、改善生态环境已成为全人类的共识。
①在煤中加入适量的石灰石作脱硫剂,可以减少________型酸雨的发生。脱硫后产生的废料中含有的________(填化学式)可用于制造建筑材料。
②天然水中的杂质较多,常需加入明矾、氯化铁、漂白粉等处理后才能作为生活用水,氯化铁净水原理的离子方程式为________________。漂白粉能杀菌消毒,其有效成分是________________(填化学式)。
③某工业废水中含有的铊(Tl+)具有高毒性,处理时常加入NaClO溶液,将Tl+转化为Tl3+,该反应中氧化剂是________(填“Tl+”或“NaClO”),同时加入适量氨水以调节水体的pH,从而将Tl3+转化为难溶的________(填化学式)沉淀除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中进行的反应:P(g)+ Q(g)![]() R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( )
R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( )
A. P、Q、R、S的浓度相等
B. P、Q、R、S在密闭容器中共存
C. P、Q、R、S的浓度不再变化
D. 用P的浓度表示的化学反应速率与用Q的浓度表示的化学反应速率相等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中,发生反应X(g)+2Y(g)![]() 3Z(g)△H=-akJ·mol-1(a>0),下列说法正确的是
3Z(g)△H=-akJ·mol-1(a>0),下列说法正确的是
A. 容器内气体的压强不再发生变化,说明反应达到平衡状态
B. 达到化学平衡状态时,反应放出的总热量可能为akJ
C. 当X、Y、Z的浓度之比为1:2:3时,反应达到化学平衡状态
D. 降低反应温度,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某同学设计的木炭和浓硫酸反应并检验所得全部产物的实验装置.已知酸性高锰酸钾溶液具有强氧化性,可将S元素从+4价氧化为+6价.请回答: 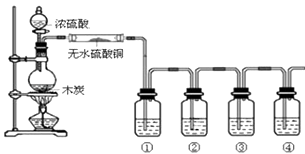
(1)装置中盛浓硫酸的仪器名称是;实验过程中大玻璃管内无水硫酸铜表面的现象是;图中4个洗气瓶装有的试剂请从下列药品中选择:澄清石灰水;酸性高锰酸钾溶液;品红溶液;(可重复选用)试指出各洗气瓶内试剂名称① , ② , ③ , ④ .
(2)检验所得产物含SO2的实验现象为
(3)检验所得产物含CO2的实验现象为 .
(4)写出木炭和浓硫酸反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧元素和硫元素组成的两种物质发生化学反应的微观示意图如下所示,其中●表示硫原子,○表示氧原子. 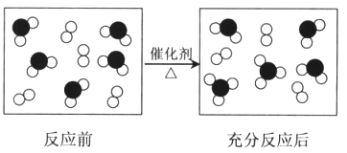
请回答下列问题:
(1)该反应的化学方程式是 .
(2)反应过程中,O2的浓度在5min内由5mol/L变成了1mol/L,用O2表示的化学反应速率是mol/(Lmin).
(3)在等温等容条件下,该反应达到化学平衡状态的依据是(填序号).
a.容器中压强不再改变
b.混合气体中c(O2)不再改变
c.c(SO2)=c(O2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com