
【题目】为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1 g样品加热,其质量变为w2 g,则该样品中Na2CO3的纯度(质量分数)是
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的有几个( )
①在常温常压下,1mol氦气含有原子数为2NA
②0.5molO2和0.5molO3的混合物所含有的氧原子个数为2.5NA
③常温常压下,18 g H2O中含有的原子总数为3NA
④常温常压下,2.24 LCO和CO2混合气体中含有的碳原子数目为0.1NA
⑤含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol·L-1
⑥1.00 mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023
⑦1 mol·L-1 NaCl溶液含有NA个Na+
⑧常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
⑨13.5g Al与足量盐酸反应生成H2的分子数为NA
⑩标准状况下,2.24LCH4所含电子数为NA
A.3 B.4 C.5 D.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的量和摩尔质量的叙述,正确的是( )
A.水的摩尔质量是18 g
B.0.012 Kg 12C中约含有6.02×1023个碳原子
C.1 mol水中含有2 mol氢和1 mol氧
D.1 mol任何物质都含有6.02×1023个分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G、H、I九种物质,其中A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G、F是单质,其余均为化合物,H是一种淡黄色固体,它们的转化关系如图所示。请回答:

(1)画出G离子结构示意图________;
(2)写出B、I的化学式B________,I________;
(3)写出H的一种用途__________________________________;
(4)写出A受热分解的化学方程式_________________________;
(5)若H与C反应固体增重4.2 g,则参加反应的C气体在标准状况下的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是三种金属,根据下列①、②两个实验,确定它们的还原性强弱顺序为( ) ①将A与B浸在稀硫酸中用导线相连,A上有气泡逸出,B逐渐溶解;
②使用惰性电极电解物质的量浓度相同的A、C混合盐溶液,阴极上先析出C.
A.A>B>C
B.B>C>A
C.C>A>B
D.B>A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸锰(MnCO3)是理想的高性能强磁性材料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,广泛用于电子、化工、医药等行业。
(1)工业上制备方程式为:MnSO4+2NH4HCO3=MnCO3↓+(NH4)2SO4+CO2↑+H2O。反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4.加入稍过量的NH4HCO3的目的是 。
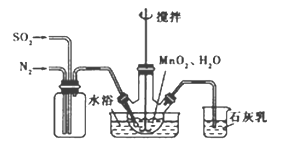
(2)实验室模拟工业二氧化锰制备硫酸锰装置如图
①石灰乳参与反应的化学方程式为 。
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有 。
(3)MnCO3在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示。则300℃时,剩余固体中n(Mn)∶n(O)为 ;图中点D对应固体的成分为 (填化学式)。
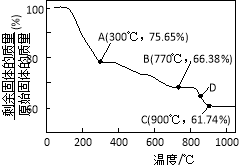
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所含分子数由多到少的排列顺序是 (用字母排序)
A.标准状况下33.6LH2
B.所含电子的物质的量为4mol的H2
C.20℃时45gH2O
D.常温下,16gO2与14gN2的混合气体
E.含原子总数约为1.204×1024的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,F是海水中含有盐的主要成分,J为D、G反应产物形成的水溶液。
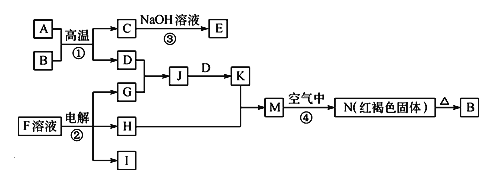
请回答下列问题:
(1)B的化学式为 。
(2)H的电子式为 。
(3)写出反应②的离子方程式 。
(4)写出反应④的化学方程式 。
(5)D是目前应用最广泛的金属,D与炭混合物在水溶液中可形成许多微电池。将含有Cr2O72–的酸性废水通过该混合物,在微电池 极上Cr2O72–转化为Cr3+,其电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、硅元素的单质及其化合物是构成自然界的重要物质。
(1)甲烷是最简单的有机物,实验室可通过下列反应制取:
CH3COONa+NaOH![]() CH4↑+X(已配平)
CH4↑+X(已配平)
①X属于 晶体(填晶体类型);
②MgO晶体的熔点比CaO高,主要原因是 。
(2)C60、金刚石和石墨是三种重要的碳单质,结构模型分别如下图所示(其中石墨仅表示出其中的一层结构)。
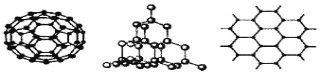
①金刚石中碳原子的杂化方式为 ;
②石墨层状结构中,平均每个正六边形占有的C—C键数是 个。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com