
| A. | 升高温度,溶液的pH降低 | |
| B. | 加入少量NaOH固体,c(SO32- )与c(Na+)均增大 | |
| C. | c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-) | |
| D. | c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3) |
分析 A、升高温度,会促进盐的水解;
B、根据水解平衡的移动原理分析,氢氧化钠抑制亚硫酸根离子的水解;
C、根据溶液中的电荷守恒知识来回答;
D、根据溶液中的物料守恒知识来回答.
解答 解:0.1mol•L-1 Na2SO3溶液中存在水解平衡:SO32-+H2O?HSO3-+OH-,该过程是吸热过程.
A、升高温度,水解平衡正向移动,所以溶液的pH升高,故A错误;
B、加入少量NaOH固体,平衡:SO32-+H2O?HSO3-+OH-向逆反应方向移动,所以c(SO32-)与c(Na+)均增大,故B正确;
C、溶液中存在电荷守恒:c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-),故C正确;
D、溶液中存在物料守恒:c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3),故D错误;
故选:BC.
点评 本题考查学生盐的水解平衡移动原理以及溶液中的离子之间的守恒关系知识,难度不大.


科目:高中化学 来源: 题型:选择题
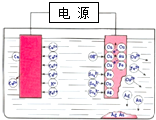
| A. | 右边电极材料为精铜 | |
| B. | 电解质溶液可选择CuSO4溶液 | |
| C. | 随着电解的进行,溶液中Cu2+浓度逐渐增加 | |
| D. | 阳极质量的减小量等于阴极质量的增加量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅溶于水显酸性 | |
| B. | 光导纤维传导光的能力非常强,利用光缆通讯,能同时传送大量信息 | |
| C. | 因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强 | |
| D. | 作为宇航用的复合材料中,常用作基体的金属是镁、铝钛等黑色金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 | |
| B. | 常用的二次电池铅蓄电池充电时电池正极与电源负极相接 | |
| C. | 用铂电极电解CuSO4溶液,当Cu2+浓度降低至原来一半时,加入CuO使溶液恢复到原来浓度和质量 | |
| D. | 在轮船船壳吃水线下焊上铜块可避免船体遭受腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种元素的最高正价氧化物的相应水化物之间能两两反应 | |
| B. | Ym+的半径最小 | |
| C. | Y元素一定是金属元素 | |
| D. | 原子半径:Z>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用滴定管取所用药品 | |
| B. | NaOH溶液在倒入小烧杯时,有少量溅出 | |
| C. | 大小烧杯体积相差较大,夹层间放的碎泡沫塑料较多 | |
| D. | 测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1 mol•L-1醋酸溶液中:c(H+)=c(CH3COO- )+c(OH- ) | |
| B. | 饱和小苏打溶液中:c(Na+)=c(HCO3-) | |
| C. | 氯化铵溶液:c(NH+4)>c(Cl-)>c(H+)>c(OH-) | |
| D. | pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com