
【题目】现有阳离子交换膜、阴离子交换膜、石墨电极和如图所示的电解槽。用氯碱工业中的离子交换膜技术原理,可电解Na2SO4溶液生产NaOH溶液和H2SO4溶液。下列说法中正确的是( )
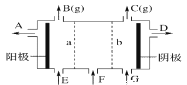
A.b是阳离子交换膜,允许Na+通过
B.从A口出来的是NaOH溶液
C.阴极反应式为4OH--4e-= 2H2O+O2↑
D.Na2SO4溶液从G口加入
科目:高中化学 来源: 题型:
【题目】常温下,XOH、YOH及ZOH三种一元碱的物质的量浓度均为0.100 mol·L-1,体积均为10.00 mL,分别用0.100 mol·L-1的HCl溶液滴定,滴定曲线如图所示。下列说法正确的是
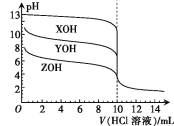
A.均可用酚酞作指示剂
B.电离平衡常数:Kb(YOH)<Kb(ZOH)
C.均滴入10.00 mL HCl溶液时,ZCl溶液中的水解程度最大
D.pH=11的YOH与pH=3的HCl溶液等体积混合:c(Cl-)>c(Y+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种碳酸饮料中主要含柠檬酸、碳酸、白砂糖、苯甲酸钠等成分,常温下测得其pH约为![]() ,下列说法不正确的是
,下列说法不正确的是![]()
A.柠檬酸的电离会抑制碳酸的电离
B.该碳酸饮料中水的电离受到抑制
C.常温下,该碳酸饮料中![]() 的值大于纯水中
的值大于纯水中![]() 的值
的值
D.打开瓶盖冒出大量气泡,是因为压强减小,降低了![]() 的溶解度
的溶解度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表中第四周期的部分元素![]() 从左到右按原子序数递增排列
从左到右按原子序数递增排列![]() ,根据要求回答下列问题:
,根据要求回答下列问题:
K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(1)以上元素的基态原子的电子排布中,4s轨道上只有1个电子的元素有______![]() 填元素名称
填元素名称![]() 。
。
(2)以上元素中,属于s区的元素有_________种,属于d区的元素有______种。
(3)第一电离能![]() ________
________![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”,下同
”,下同![]() 。
。
(4)现有含钛的两种颜色的晶体,![]() 的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为
的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为![]() 。为测定这两种晶体的化学式,设计了如下实验:
。为测定这两种晶体的化学式,设计了如下实验:
![]() 分别取等质量的两种配合物晶体的样品配成待测溶液;
分别取等质量的两种配合物晶体的样品配成待测溶液;
![]() 分别往待测溶液中滴入
分别往待测溶液中滴入![]() 溶液,均产生白色沉淀;
溶液,均产生白色沉淀;
![]() 溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的
溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的![]() 。试推断紫色晶体的化学式为_________。
。试推断紫色晶体的化学式为_________。
(5)含有元素K的盐的焰色反应为__________色。许多金属盐都可以发生焰色反应,其原因是____________。
(6)立方氮化硼晶体![]() ,是一种超硬材料,有优异的耐磨性,其晶胞如图所示。
,是一种超硬材料,有优异的耐磨性,其晶胞如图所示。
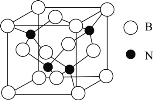
若立方氮化硼晶胞的边长为![]() ,则立方氮化硼的密度为________g/cm3
,则立方氮化硼的密度为________g/cm3![]() 只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。
只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
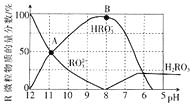
【题目】室温下,向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 盐酸,溶液含R微粒的物质的量分数与pH关系如图所示
盐酸,溶液含R微粒的物质的量分数与pH关系如图所示![]() 不稳定,易转化为
不稳定,易转化为![]() 气体逸出溶液,气体逸出未画出,忽略因气体逸出引起的溶液体积变化
气体逸出溶液,气体逸出未画出,忽略因气体逸出引起的溶液体积变化![]() 下列说法错误的是
下列说法错误的是![]()
A.![]() 溶液中:
溶液中:![]()
B.当溶液![]() 时,溶液总体积大于40mL
时,溶液总体积大于40mL
C.在B点对应的溶液中,离子浓度最大的是![]()
D.A点对应pH约为![]() ,
,![]() 的水解常数
的水解常数![]() 数量级为
数量级为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、根据氧化还原反应:2Ag+(aq)+ Cu(s) = Cu2+(aq)+ 2Ag(s) 设计的原电池如下图所示,其中盐桥为琼脂–饱和KNO3盐桥。请回答下列问题:
(1)电极X的材料是 ___________;电解质溶液Y是 ____________________。
(2)银电极为电池的 __________ 极,其电极反应式为:___________________________________ 。
(3)盐桥中向CuSO4溶液中迁移的离子是 ___________。

A、K+ B、NO3― C、Ag+ D、SO42―
Ⅱ、酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料。回答下列问题:
(1)该电池的正极反应式为 ________________________,电池反应的离子方程式为________________________________________
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过 ___________________________________ 分离回收。
(3)滤渣的主要成分是MnO2、碳粉和MnOOH,欲从中得到较纯的MnO2,最简便的方法是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解装置如图所示:

Ⅰ.当用惰性电极电解时,c为____________极, d极的电极反应_________,电解总反应的化学方程____________________
Ⅱ.(1)若用此装置进行铁上镀铜则c为__________(填铁或铜),电解液浓度_____________(增大,减小或不变)
(2)电镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子___________mol.
Ⅲ.若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极________(填图中的字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A. 1mol甲基含10NA个电子
B. 15 g C2H6中含有共价键数目为3NA
C. 标准状况下,11.2 L三氯甲烷所含的分子数目为0.5NA
D. 一定条件下,2.6 g苯和苯乙烯的混合物完全燃烧消耗O2的分子数为0.25NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将不同物质的量的M(g)和N(g)分别通入体积为2L的恒容密闭容器中,进行反应M(g)+N(g)![]() P(g)+Q(g),得到如下两组数据:
P(g)+Q(g),得到如下两组数据:

下列说法正确的是( )
A.将实验2的体积压缩为1L,c(Q)为0.4molL-1
B.温度升高,该反应的平衡常数增大
C.选择合适的催化剂可降低该反应的活化能,提高M的转化率
D.实验1中M的化学反应速率为0.32molL-1min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com