
| A. | 铁与Cl2、盐酸均能发生反应,但生成的含铁物质组成不同 | |
| B. | 分别加热蒸干并灼烧铁、铝的氯化物溶液,最后得到的物质均为金属氧化物 | |
| C. | 等物质的量的Na、Cu、Al与足量氯气反应时,消耗的氯气一样多 | |
| D. | 常温下,铁片、铝片与浓硫酸的反应均只能停留在金属的表面上 |
分析 A.铁与氯气反应生成氯化铁,与盐酸反应生成氯化亚铁;
B.加热促进氯化铝、氯化铁水解,且氯化氢具有挥发性;
C.根据Na、Cu、Al与足量氯气反应分析;
D.依据浓硫酸具有强的氧化性,常温下能够使铁、铝发生钝化.
解答 解:A.铁与氯气反应生成氯化铁,与盐酸反应生成氯化亚铁,所以生成的含铁物质组成不同,故A正确;
B.加热促进氯化铝、氯化铁水解,且氯化氢有挥发性,导致蒸干时得到氢氧化铝、氢氧化铁固体,再将固体灼烧,氢氧化铝分解生成氧化铝和水,氢氧化铁分解生成氧化铁和水,则最后得到的固体都是氧化物,故B正确;
C.因为2Na~Cl2,Cu~Cl2,2Al~3Cl2,等物质的量的Na、Cu、Al与氯气反应,消耗的氯气为Al>Cu>Na,故C错误;
D.浓硫酸具有强的氧化性,常温下能够使铁、铝发生钝化,形成致密氧化膜,阻止反应进行,故D正确;
故选:C.
点评 本题考查了元素化合物知识,熟悉铁、浓硫酸性质,盐类水解规律是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
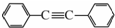 .以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
.以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下: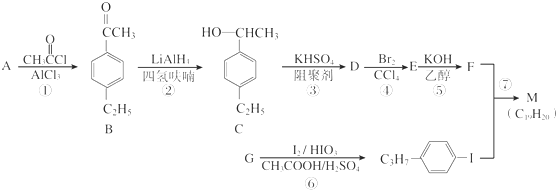
 .
. .
.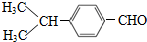 (写结构简式).
(写结构简式).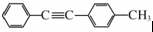 的合成路线:
的合成路线: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,电子由正极通过外电路流向负极 | |
| B. | 电池正极的电极反应式为:MnO2(s)+H2O(l)+e-═MnOOH(s)+OH-(aq) | |
| C. | 电池工作时,锌发生氧化反应 | |
| D. | 当电路中通过0.2mol电子,锌的质量理论上减小6.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol N2所含有的原子数为NA | |
| B. | 标准状况下,22.4 L水中含有的水分子数为NA | |
| C. | 24 g O2分子和24 g O3分子所含的氧原子数目相等 | |
| D. | 1mol•L-1的盐酸中氯离子为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有羟基的有机物都能与醋酸发生酯化反应 | |
| B. | 氨基酸、乙酸和苯酚都能与氢氧化钠溶液反应 | |
| C. | 醇类、卤代烃都能发生消去反应 | |
| D. | 除饱和烃之外的其他烃都能发生聚合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
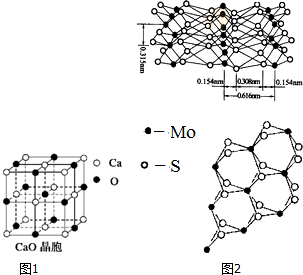 决定物质性质的重要因素是物质结构.请回答下列问题.
决定物质性质的重要因素是物质结构.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
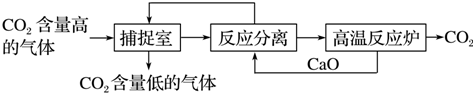
| A. | 生产过程中,可循环利用的物质有CaO和NaOH | |
| B. | 该方法涉及了化合、分解和复分解等反应类型 | |
| C. | 该方法通过化学变化,分离、提纯并利用CO2,可以减少碳的排放 | |
| D. | “反应分离”环节中,分离物质的基本操作是蒸发、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH 加成反应 | |
| B. | 2CH3CH2OH $?_{140℃}^{浓硫酸}$CH3CH2OCH2CH3+H2O 消去反应 | |
| C. | 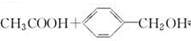 $?_{△}^{浓硫酸}$ $?_{△}^{浓硫酸}$ 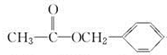 +H2O取代反应 +H2O取代反应 | |
| D. | 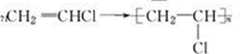 加聚反应 加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 | |
| C. | 向水中加入少量固体NaOH,平衡逆向移动,c(H+)降低,KW减小 | |
| D. | 将水加热,KW增大,pH不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com