
| A. | 同周期元素中,X氢化物的沸点最高 | |
| B. | 简单离子半径:X>Y>Z | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
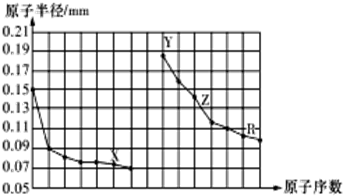
分析 同周期自左而右原子半径减小,同主族自上而下原子半径增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为O元素,Y为Na元素,Z为Al元素,R为S元素,结合元素周期律与物质的性质等解答.
解答 解:同周期自左而右原子半径减小,同主族自上而下原子半径增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为O元素,Y为Na元素,Z为Al元素,R为S元素.
A.X为O元素,非金属性比F弱,第二周期中HF的稳定性最强,故A错误;
B.X为O元素,Y为Na元素,Z为Al元素,简单离子的半径:O2->Na+>Al3+,故B正确;
C.Y、Z、R对应的最高价氧化物的水化物分别为:NaOH、Al(OH)3、H2SO4,氢氧化钠与硫酸发生中和反应,氢氧化铝属于两性氢氧化物,能与氢氧化钠、硫酸反应,故C正确;
D.工业上电解熔融的Al2O3冶炼Al,故D正确;
故选A.
点评 本题考查位置结构性质的关系及应用,题目难度中等,推断元素是解题的关键,根据原子半径变化规律结合原子序数进行推断,首先审题中要抓住“短周期主族元素”几个字.


科目:高中化学 来源: 题型:选择题
| A. | H2O2分子的空间构型为直线形 | |
| B. | CO2分子为非极性分子 | |
| C. | BF3分子中的B原子满足8电子稳定结构 | |
| D. | CH3COOH分子中C原子均为sp2杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 仪器 | 药品 | 实验目的 |
| A | 烧杯、玻璃棒、胶头滴管 | FeCl3溶液、NaOH溶液 | 制Fe(OH)3胶体 |
| B | 圆底烧瓶、导气管、烧杯、铁架台 | 干燥的二氧化碳、蒸馏水 | 模拟喷泉实验 |
| C | 酸式滴定管、锥形瓶、铁架台(带铁夹) | 已知浓度的盐酸,待测NaOH溶液 | 测定NaOH溶液的物质的量浓度 |
| D | 酒精灯、玻璃棒、蒸发皿、三脚架 | NaCl溶液 | 蒸发溶液得到晶体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
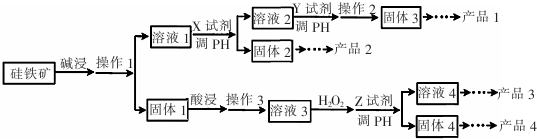
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑥ | B. | ②⑤ | C. | ①②⑤⑥ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40 mL | B. | 72 mL | C. | 128 mL | D. | 20 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com