
������ԭ��Ӧ�У�ˮ�����ÿ���������������ԭ�����������������ǻ�ԭ�����ȷ��������ַǻ�ԭ���ȡ����з�Ӧ��Br2+SO2+2H2O=H2SO4+2HBr��Ƚϣ�ˮ�����ò���ͬ���� �� ��
��2Na2O2+2H2O=4NaOH+O2��
��4Fe��OH��2+O2+2H2O=4Fe��OH��3
��2F2+2H2O=4HF+O2
��2Al+2NaOH+2H2O=2NaAlO2+3H2��
A���٢� B���ڢ� C���ڢ� D���ۢ�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��������������������ظ�һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����100ml 1mol/LCaCl2��Һ��������ȷ����
A��Cl-�����ʵ���Ũ��Ϊ2mol/L
B��CaCl2�����ʵ���Ϊ1mol
C��ȡ��50 mL��ʣ����Һ��CaCl2�����ʵ���Ũ��Ϊ0.5mol/L
D������Һ��ˮ�����Ϊ100 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ɽ�϶��и߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
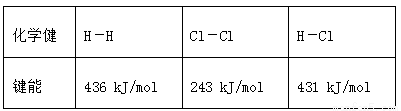
ͨ�����ǰѲ�1 molij��ѧ�������յ��������γ�1 molij��ѧ�����ͷŵ����������û�ѧ���ļ��ܣ����ܵĴ�С�����ڹ��㻯ѧ��Ӧ�ķ�Ӧ�ȣ���H������֪
��ѧ�� | H��H | Cl��Cl | H��Cl |
���� | 436 kJ/mol | 243 kJ/mol | 431 kJ/mol |
��ѧ�� | H��H | Cl��Cl | H��Cl |
���� | 436 kJ/mol | 243 kJ/mol | 431 kJ/mol |
������ �Ȼ�ѧ����ʽ����ȷ���ǣ� ��
�Ȼ�ѧ����ʽ����ȷ���ǣ� ��
A��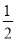 H2��g����
H2��g���� 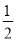 Cl2��g��===HCl��g�� ��H��+91.5 kJ��mol��1
Cl2��g��===HCl��g�� ��H��+91.5 kJ��mol��1
B��H2��g����Cl2��g��===2HCl��g�� ��H����183 kJ��mol��1
C��2HCl��g��===H2��g����Cl2��g�� ��H��+18 3 kJ��mol��1
3 kJ��mol��1
D��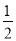 H2��g����
H2��g����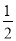 Cl2��g��===HCl��g�� ��H����91.5 kJ��mol��1
Cl2��g��===HCl��g�� ��H����91.5 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ��УЭ�����һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
ˮ�ȷ���ֱ��Ϊ1��100 nm�Ŀ���Y�����������Ӧԭ��Ϊ��3Fe2+ + 2S2O32- + O2 + aOH��= Y+ S4O62- + 2H2O������˵���в���ȷ���ǣ� ��
A��a=4
B��S2O32-�ǻ�ԭ��
C����Y���ȷ�ɢ��ˮ���γɵ���ϵ���ж����ЧӦ
D��ÿ��3 mol Fe2+ �μӷ�Ӧ����Ӧ��ת�Ƶĵ�������Ϊ5 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ��УЭ�����һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ���ǣ� ��
A��ʯ��ˮ�����̼��������Һ��Ӧ��HCO3����Ca2����OH��=CaCO3����H2O
B������������Һ�м�������������Һ�����ԣ�2H����SO42����Ba2����2OH��=BaSO4����2H2O
C������ͭ��ϡ���ᷴӦ��2H����O2��=H2O
D��̼��������Һ�м������CO32����2H��=CO2����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ��УЭ�����һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ṩʵ�����ģ������������ޣ����������Ӧʵ���һ���ǣ� ��
ʵ�����ģ�ʡ�Լг�װ�ã� | ��Ӧʵ�� | |
A | �ձ����������������� | �Ȼ�����Һ�������ᾧ |
B | �ձ�������������ͷ�ιܡ���ֽ | �������ȥ���������е�����̼��� |
C | �ձ�������������ͷ�ιܡ�����ƿ | �ù�������������0.1 mol/L����Һ |
D | �ձ�������������ͷ�ιܡ���Һ©�� | ����ˮ��CCl4��ȥNaBr��Һ�е�����NaI |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ����У��һ�����л�ѧ���������棩 ���ͣ������
3Cu+8H����+2NO3��3Cu2��+2NO��+4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ������ʮ��У��һ�����л�ѧ���������棩 ���ͣ�ʵ����
ʵ�����ڼ���������H2��ԭCuO���õĺ�ɫ���������Cu��Cu2O�Ļ�����֪Cu2O��������Һ�пɷ�������������ԭ��Ӧ������Cu2+�͵���ͭ������8g CuO��H2��ԭ�õ���ɫ����6.8g��
��1��д��H2��ԭCuO����Cu2O�Ļ�ѧ����ʽ ��
��2��6.8 g����������к�Cu��Cu2O�����ʵ���֮���� ��
��3������6.8 g�����������������ϡ�����ַ�Ӧ����ˣ��ɵõ��� �� g
�� g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡޭ���ظ߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
T��ʱ����2L�����ܱ���������̬����X��Y��Z�����ʵ�����ʱ��仯�IJ������������ʾ��
T/min | n��X�� /mol | n��Y�� /mol | n��Z�� /mol |
0 | 0.80 | 1.00 | 0 |
1 | 0.70 | 0.80 | 0.20 |
5 | 0.70 | ||
9 | 0.40 | ||
10 | 0.40 | 0.80 |
��1��д���÷�Ӧ�Ļ�ѧ����ʽ_________________
��2����Ӧ���е�10min��X��ת����Ϊ___________��0~5min��Y��ƽ����Ӧ����Ϊ___________
��3������T��ʱ�÷�Ӧ��ƽ�ⳣ��K=____________
��4��T��������ܱ�������ͨ��һ������X��Y��Z����Ӧ��ijʱ�̲��X��Y��Z�����ʵ����ֱ�Ϊ1.00mol��0.50mol��1.60mol�����ʱ���淴Ӧ���ʴ�С��v�� v�棨����ڡ��������ڡ�����С�ڡ���
��5������10min��t3��t5ʱ�̷ֱ�ı�÷�Ӧ��ijһ��Ӧ�������õ�X��Z�����ʵ�������Ӧ������ʱ��Ĺ�ϵ����ͼA��B��ʾ��
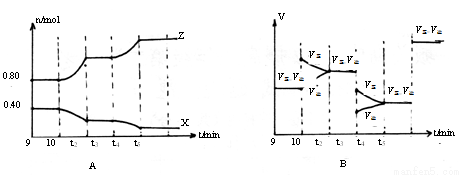
10minʱ�ı�ķ�Ӧ������_______________
��t3ʱ�̸ı�ķ�Ӧ������_______________
��t5ʱ�̸ı�ķ�Ӧ������ ��������___________________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com