
科目:高中化学 来源: 题型:
(12分)、高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
已知:① 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 → 5KCl + KClO3+ 3H2O(条件:温度较高)
③ 2Fe(NO3)3 + 2KClO + 10KOH→ 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
⑴该生产工艺应在 __ (填“温度较高”或“温度较低”)的情况下进行;
⑵写出工业上制取Cl2的化学方程式 __ ;
⑶配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为 __ ;
⑷在“反应液I”中加KOH固体的目的是 __ :
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物 D.使副产物KClO3转化为 KClO
⑸从“反应液II”中分离出K2FeO4后,会有副产品 _ (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途 _ 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市日坛中学高一上学期期中考试化学试卷(带解析) 题型:实验题
(10分)
某实验需要100 mL、0.1 mol/L的Na2CO3溶液,现通过如下操作配制:
①把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用 (填仪器名称)搅拌
②把①所得溶液冷却到室温后,小心转入 (填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用 (填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是 (填序号)。
(2)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为 。
(3)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) ="0.01" mol/L的溶液,则稀释后溶液的体积为 mL
(4)在配制100 mL、0.1 mol/L的Na2CO3溶液时,下列操作中的 会导致结果偏低(请用
序号填写)
a.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
b.定容时俯视刻度线
c.定容时仰视刻度线
d.干净的容量瓶未经干燥就用于配制溶液
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省东莞市高三上学期第一次月考理综化学试卷(解析版) 题型:实验题
(15分)某实验需要100 mL、1 mol/L的Na2CO3溶液,现通过如下操作配制:
① 把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用 (填仪器名称)搅拌
②把①所得溶液冷却到室温后,小心转入 (填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用 (填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是 (填序号)。
(2)若没有操作④,则所配溶液的浓度会 (填“偏高”或“偏低”)。
(3)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为 。
(4)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) =0.01 mol/L的溶液,则稀释后溶液的体积为 mL
(5)在配制100 mL、1 mol/L的Na2CO3溶液时,下列操作中的 会导致结果偏低(请用序号填写)
①用拖盘天平称量时砝码放在左盘
②将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
③定容时俯视刻度线
④定容时仰视刻度线
⑤干净的容量瓶未经干燥就用于配制溶液
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省高三11月练习化学试卷 题型:填空题
(12分)、高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
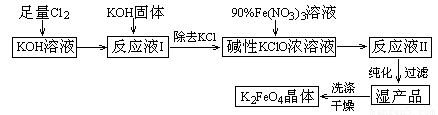
已知:① 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 → 5KCl + KClO3 + 3H2O(条件:温度较高)
③ 2Fe(NO3)3 + 2KClO + 10KOH → 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
⑴该生产工艺应在 __ (填“温度较高”或“温度较低”)的情况下进行;
⑵写出工业上制取Cl2的化学方程式 __ ;
⑶配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为 __ ;
⑷在“反应液I”中加KOH固体的目的是 __ :
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物 D.使副产物KClO3转化为 KClO
⑸从“反应液II”中分离出K2FeO4后,会有副产品 _ (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途 _ 。
查看答案和解析>>
科目:高中化学 来源:2014届湖北省武汉市高一上学期期中联考化学试卷 题型:实验题
某实验需要100 mL、1 mol/L的Na2CO3溶液,现通过如下操作配制:
① 把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用 (填仪器名称)搅拌 ②把①所得溶液冷却到室温后,小心转入 (填仪器名称)③继续加蒸馏水至液面至刻度线1~2cm处,改用 (填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切 ④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀 ⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是 (填序号)。
(2)若没有操作④,则所配溶液的浓度会 (填“偏高”或“偏低”)。
(3)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为 。
(4)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) =0.01 mol/L的溶液,则稀释后溶液的体积为 mL
(5)在配制100 mL、1 mol/L的Na2CO3溶液时,下列操作中的 会导致结果偏低(请用序号填写)
①用拖盘天平称量时砝码放在左盘
②将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
③定容时俯视刻度线
④定容时仰视刻度线
⑤干净的容量瓶未经干燥就用于配制溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com