
| A. | 1 mol任何气体的体积都约为22.4L | |
| B. | 将1L 10 mol/L的浓盐酸与9L水混合时物质的量浓度为1 mol/L | |
| C. | 将22.4L氯化氢气体溶于水配成1L溶液时物质的量浓度为1 mol/L | |
| D. | 标准状况下,22.4L的任何气体的物质的量都是1 mol |
分析 A、气体摩尔体积22.4L/mol的使用条件是标准状况;
B、根据不同液体混合时体积能否直接加和判断;
C、未指明是标准状况,22.4L氯化氢气体不一定为1mol;
D、标准状况下,气体摩尔体积22.4L/mol,则22.4L的任何气体的物质的量都是1mol.
解答 解:A、未指明是标准状况,不能使用气体摩尔体积22.4L/mol,所以1 mol任何气体的体积不一定约为22.4L,故A错误;
B、1L10mol/L的浓盐酸与9L水混合配成溶液的体积不是10L,所以混合后溶液的物质的量浓度不是1mol/L,故B错误;
C、气体摩尔体积受温度和压强的影响,温度越高,气体摩尔体积越大,标况下,22.4LHCl的物质的量是1mol,常温常压下,22.4LHCl的物质的量小于1mol,所以未指明是标准状况,22.4L氯化氢气体不一定为1mol,溶于水配成1L的盐酸溶液的物质的量浓度也不一定是1mol/L,故C错误;
D、标准状况下,气体摩尔体积22.4L/mol,则22.4L的任何气体的物质的量都是1mol,故D正确.
故选D.
点评 本题考查气体摩尔体积的适用条件和范围,只有在标况下的气体才适用,比较容易.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:选择题
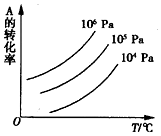 有一化学平衡mA(g)+nB(g)?pC(g)+qD(g),如图所示是A的转化率同压强、温度的关系,分析图3可以得出的正确结论是( )
有一化学平衡mA(g)+nB(g)?pC(g)+qD(g),如图所示是A的转化率同压强、温度的关系,分析图3可以得出的正确结论是( )| A. | 正反应吸热,m+n>p+q | B. | 正反应吸热,m+n<p+q | ||
| C. | 正反应放热,m+n>p+q | D. | 正反应放热,m+n<p+q |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①②④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制稀盐酸用量筒量取浓盐酸时,俯视刻度线 | |
| B. | 用量筒量取所需的浓盐酸倒入烧杯后,再用水洗量筒2-3次,洗液倒入烧杯中 | |
| C. | 称量11.7 g NaCl配制0.2 mol/L NaCl溶液时,砝码错放在左盘 | |
| D. | 定容时仰视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 上述电池分别属于一次电池、二次电池和燃料电池 | |
| B. | 干电池在长时间使用后,锌筒被破坏 | |
| C. | 氢氧燃料电池是一种具有应用前景的绿色电源 | |
| D. | 铅蓄电池工作过程中,每通过 2 mol 电子,负极质量减轻 207 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com