
化学与生产、生活密切相关,下列叙述中正确的是
A.用活性炭为糖浆脱色和用双氧水漂白纸浆,其原理相同
B.铜制品在潮湿空气中生锈,其主要原因是发生析氢腐蚀
C.用NaHCO3和Al2(SO4)3溶液可以制作泡沫灭火剂
D.从海水中可以制取NaCl,电解饱和NaCl溶液可以制取金属Na
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:选择题
短周期元素A、B、C、D的原子序数依次增大,它们原子的最外层电子数之和为16,A与D同主族,B+与A2-具有相同的电子层结构,C原子的最外层电子数等于A原子最外层电子数的一半,则下列叙述正确的是
A.B2A2和B2A中阴阳离子的个数比相同
B.原子半径的大小顺序:r(D)>r(C)>r(B)>r(A)
C.D的简单气态氢化物的热稳定性比A的强
D .元素C的单质是一种高硬度、高熔点的金属
.元素C的单质是一种高硬度、高熔点的金属
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长沙市高三4月月考理综化学试卷(解析版) 题型:选择题
近几年科学家发明的一种新型可控电池——锂水电池,工作原理如图所示。下列有关说法不正确的是
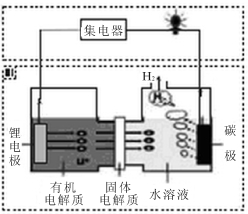
A.碳极发生的反应是:2H2O+2e-=H2↑+2OH-
B.有机电解质和水溶液不可以互换区域
C.标况下产生22.4L的氢气时,正极消耗锂的质量为14g
D.该装置不仅可提供电能,还可得到清洁的氢气
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高三3月教学质量监测理综化学试卷(解析版) 题型:推断题
【化学——选修5:有机化学基础】(15分)F(聚碳酸酯)是一种性能优良的工程塑料,合成路线如下:
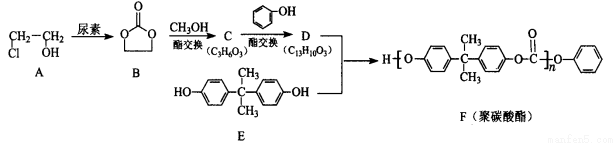
已知:
(1)C的结构简式是_____________________;D的结构简式是____________________。
(2)B→C的反应类型为__________________;D+E生成F的反应类型为_____________。
(3)图中B(碳酸乙烯酯)也可通过下列反应制备:
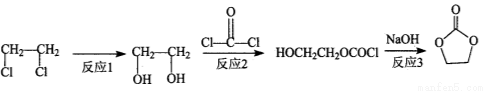
①反应1的试剂和条件为________________________________________。
②反应2的反应类型是_________________________________________。
③反应3的化学方程式为________________________________。
(4)C的核磁共振氢谱有______________组峰;C的一种同分异构体,能发生银镜反应和水解反应,该同分异构体的结构简式为____________________________。
(5)D有多种同分异构体,符合下列条件的有_____________种。
①有萘环(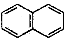 )结构
)结构
②两个醛基且在一个环上
③一个羟甲基(一CH2OH)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省新校高三4月模拟化学试卷(解析版) 题型:简答题
(15分)CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气。
(1)已知:CH4、H2和CO的燃烧热(△H)分别为-890.3kJ/mol、-285.8kJ/mol和-283.0kJ/mol,且1mol液态水汽化时的能量变化为44.0kJ。用1 m3(标准状况)的甲烷与水蒸气在高温下反应制取合成气所需的热量为 (保留整数)。
(2)在一定温度下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),测得CH4(g)和H2(g)的物质的量浓度随时间变化如下表所示:
物质浓度 时间/min | 0 | 1 | 2 | 3 | 4 |
CH4 | 0.2mol·L-1 | 0.13 mol·L-1 | 0.1 mol·L-1 | 0.1 mol·L-1 | 0.09 mol·L-1 |
H2 | 0 mol·L-1 | 0.2 mol·L-1 | 0.3 mol·L-1 | 0.3 mol·L-1 | 0.33 mol·L-1 |
①计算该反应第一次达平衡时的平衡常数K 。
②3min时改变的反应条件是 (只填一种条件的改变即可)。
(3)已知温度、压强、投料比X[n(CH4)/n(H2O)]对该反应的影响如图所示。
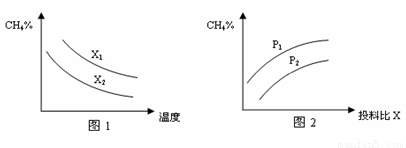
①图1中的两条曲线所示投料比的关系X1 X2(填“=”、“>”或“<”下同)。
②图2中两条曲线所示的压强比的关系:P1 P2。
(4)以天然气(设杂质不参与反应)、KOH溶液为原料可设计成燃料电池:
①放电时,负极的电极反应式为 。
②设装置中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下的体积为8.96L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省新校高三4月模拟化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.分馏、蒸馏都是物理变化,干馏、裂化、裂解都是化学变化
B.乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色
C.丹参素结构如图所示,能发生取代、加成、氧化反应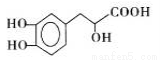
D.中和滴定实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗净后,必须干燥或润洗后方可使用
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省黄山市高三毕业班第二次质量检测理综化学试卷(解析版) 题型:选择题
根据中学所学相关知识,下列推断正确的一项是
A.ⅣA族元素形成的氢化物的沸点从上到下依次递增,则VA族元素所形成的氢化物的沸点从上到下也是依次递增
B.氯气可置换出KBr溶液中的溴,则氟气也可置换出KBr溶液中的溴
C.某浓度的NaClO溶液的pH=d则其中由水电离出的c(H-)=10-14+dmol.L-l
D.某温度下,MgCO3的KSP=6.8×10-6,则该温度下所有含固体MgCO3的溶液,都有c(Mg2+)=c(CO32-),且c(Mg2+)·c(CO32-)=6.8×10-6
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:填空题
(16分)I.(4分)已知拆开1mol H—H键,1mol N三N键分别需要吸收的能量为436kJ,946kJ;形成1mol N—H键,会放出能量391kJ,在反应N2 + 3H2== 2NH3中,每生成2mol NH3 ___ _热量(填:吸收或放出)_____ kJ。
II.(6分)我国经济发展对能源的需求与日俱增。一种新型燃料电池是将两根特制电极插入氢氧化钾溶液中,然后从两极分别通入甲烷和氧气,其电极反应式为:
X极:CH4+10OH- -8e- == CO32-+7H2O Y极:4H2O+2O2+8e- ==8OH-
(1)指出该电池的正极__________(X或Y)极
(2)在标准状况下,通入5.6L甲烷气体,完全反应后有__________mol电子转移;
(3)该电池的电解质溶液的PH变化是_______ ___(填升高、降低、不变)
III.(6分)利用Cu + 2FeCl3 = CuCl2 + 2FeCl2反应,设计一个原电池。
(1)画出装置图(在图中标出电极材料、正负极、电解质溶液)。
(2)写出电极反应方程式
负极: 正极:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com