
【题目】(14分)水泥是重要的建筑材料.水泥熟料的主要成分为CaO、SiO2 , 并含有一定量的铁、铝和镁等金属的氧化物.实验室测定水泥样品中钙含量的过程如图所示:
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸.加入硝酸的目的是 , 还可使用代替硝酸.
(2)沉淀A的主要成分是 , 其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为 .
(3)加氨水过程中加热的目的是 . 沉淀B的主要成分为、(填化学式).
(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:MnO4﹣+H++H2C2O4→Mn2++CO2+H2O.实验中称取0.400g水泥样品,滴定时消耗了0.0500molL﹣1的KMnO4溶液36.00mL,则该水泥样品中钙的质量分数为 .
【答案】
(1)将样品中的Fe2+氧化为Fe3+;H2O2
(2)SiO2;SiO2+4HF=SiF4↑+2H2O
(3)防止胶体生成,易生成沉淀;Al(OH)3;Fe(OH)3
(4)45.0%
【解析】解:(1)铁离子在pH较小时易生成沉淀,加入硝酸可氧化亚铁离子生成铁离子,比避免引入新杂质,还可用过氧化氢代替硝酸,
故答案为:将样品中的Fe2+氧化为Fe3+;H2O2;(2)由以上分析可知沉淀A为SiO2 , 不溶于强酸但可与一种弱酸反应,应为与HF的反应,方程式为SiO2+4HF=SiF4↑+2H2O,
故答案为:SiO2;SiO2+4HF=SiF4↑+2H2O;(3)滴加氨水,溶液呈碱性,此时不用考虑盐类水解的问题,加热的目的是防止生成胶体而难以分离,生成的沉淀主要是Al(OH)3、Fe(OH)3 ,
故答案为:防止胶体生成,易生成沉淀;Al(OH)3、Fe(OH)3;(4)反应的关系式为5Ca2+~5H2C2O4~2KMnO4 ,
n(KMnO4)=0.0500mol/L×36.00mL=1.80mmol,
n(Ca2+)=4.50mmol,
水泥中钙的质量分数为 ![]() ×100%=45.0%,
×100%=45.0%,
故答案为:45.0%.
水泥熟料的主要成分为CaO、SiO2 , 并含有一定量的铁、铝和镁等金属的氧化物,加入氯化铵、盐酸和硝酸,由于二氧化硅与酸不反应,则得到的沉淀A为SiO2 , 滤液中含有Fe3+、Al3+、Mg2+等离子,加入氨水调节pH4﹣5,可生成Al(OH)3、Fe(OH)3沉淀,加热的目的是防止生成胶体而难以分离,滤液主要含有Ca2+ , 加入草酸铵可生成草酸钙沉淀,加入硫酸用高锰酸钾测定,发生5Ca2+~5H2C2O4~2KMnO4 , 根据高锰酸钾的量可计算含量,以此解答该题.


科目:高中化学 来源: 题型:
【题目】(15分)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeOCr2O3 , 还含有硅、铝等杂质.制备流程如图所示:
回答下列问题:
(1)步骤①的主要反应为:FeOCr2O3+Na2CO3+NaNO3 ![]() Na2CrO4+Fe2O3+CO2+NaNO2上述反应配平后FeOCr2O3与NaNO3的系数比为 . 该步骤不能使用陶瓷容器,原因是 .
Na2CrO4+Fe2O3+CO2+NaNO2上述反应配平后FeOCr2O3与NaNO3的系数比为 . 该步骤不能使用陶瓷容器,原因是 .
(2)滤渣1中含量最多的金属元素是 , 滤渣2的主要成分是及含硅杂质.
(3)步骤④调滤液2的pH使之变(填“大”或“小”),原因是(用离子方程式表示).
(4)有关物质的溶解度如图所示.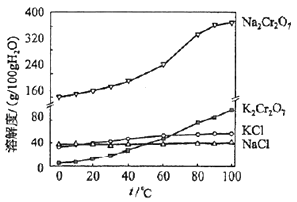
向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体.冷却到(填标号)得到的K2Cr2O7固体产品最多.
a.80℃ b.60℃ c.40℃ d.10℃
步骤⑤的反应类型是 .
(5)某工厂用m1 kg 铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7 , 最终得到产品 m2 kg,产率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的氧化物(FexO)1.52g溶于足量盐酸中,向所得溶液中通入标准状况下112mL Cl2 , 恰好将Fe2+完全氧化.下列说法正确的是( )
A.FexO溶于足量盐酸后只生成了FeCl3和H2O
B.标准状况下112 mL Cl2的物质的量是5 mol
C.x=0.8
D.通入Cl2后,发生反应的离子方程式:Fe2++Cl2=Fe3++2Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有10mL1molL﹣1 NH4Al(SO4)2溶液的烧杯中滴加1molL﹣1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下: 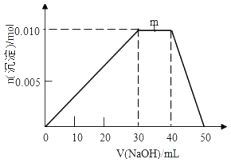
①写出m点反应的离子方程式: .
②若10mL1molL﹣1 NH4Al(SO4)2溶液中改加20mL1.2molL﹣1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为mol(列式计算)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L.向反应后的溶液中加入c mol/L 氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g.再将得到的沉淀灼烧至质量不再改变为止,得到固体p g.则下列关系正确的是( )
A.c= ![]()
B.p=m+ ![]()
C.n=m+17Vc
D.![]() m<p<
m<p< ![]() m
m
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某化学实验小组通过实验探究一红色粉末是Fe2O3、Cu2O或二者混合物.探究过程如下: Cu2O溶于稀硫酸生成Cu和CuSO4 , Cu2O在空气中加热生成Cu O
假设1:红色粉末是Cu2O
假设2:红色粉末是 Fe2O3
假设3:红色粉末是 Fe2O3、Cu2O的混合物取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN试剂
(1)若假设2成立,则实验现象是 .
(2)若滴加KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含Fe2O3 . 你认为这种说法合理吗?;简述你的理由(不需要写方程式)
(3)若固体粉末完全溶解无固体存在,滴加 KSCN试剂后溶液不变红色,则证明原固体粉末是 , 写出发生反应的离子方程式、 . 经实验分析,确定红色粉末是Fe2O3 和 Cu2O 的混合物
(4)实验小组欲用加热法测定 Cu2O 的质量分数.取 mg 固体粉末在空气中充分加热,待质量不再变化时,称其质量为n g(n>m),则混合物中Cu2O的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离或提纯物质的方法正确的是
A.用蒸发法进行海水淡化
B.用渗析的方法除去淀粉溶液中含有的少量NaCl
C.用酒精萃取碘水中的碘
D.用加热→蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.钠与水反应:Na+2H2O═Na++2OH﹣+H2↑
B.电解饱和食盐水获取烧碱和氯气:2Cl﹣+2H2O ![]() H2↑+Cl2↑+2OH﹣
H2↑+Cl2↑+2OH﹣
C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH﹣+H++SO42﹣═BaSO4↓+H2O
D.向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO3﹣+OH﹣═CaCO3↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com