
(14分)某物质用途广泛,可用作分析试剂、媒染剂、催化剂及化工原料。经测定它含有铁元素,摩尔质量为482g/mol。为进一步确定它的组成,某化学兴趣小组做了以下实验:
Ⅰ.称取48.20g该物质溶于水,配成100mL溶液,所得溶液显棕黄色。
Ⅱ.取上述溶液50mL于试管中,加入足量的0.1mol/LNaOH溶液,并加热,产生的气体经干燥后通入浓硫酸中,浓硫酸增重0.85g;产生的红褐色沉淀经过过滤、洗涤、灼烧后得4.00g固体。
Ⅲ.另取上述溶液50mL于试管中,加入足量的BaCl2溶液,产生不溶于盐酸的白色沉淀 23.30g。
请回答下列问题:
(1)实验Ⅱ中产生气体的电子式 。
(2)该物质的化学式为 ,下列有关该物质的用途合理的是 。
A.补血剂 B.净水剂 C.含酚废水的检测试剂 D.肥料
(3)该物质溶液中逐滴加入氢氧化钡溶液至金属元素完全沉淀时的化学反应方程式 。
(4)将SO2气体通入该物质的溶液中可以观察到的实验现象是 ,写出该反应的离子方程式 。
(5)为了进一步验证该物质中铁元素的化合价,某同学设计了如下实验方案:取少量固体于试管中,加水充分溶解,滴加硫氰化钾溶液,若溶液显血红色,即可证明该物质中一定存在Fe3+。请评价该实验操作是否合理 (填“合理”或者“不合理”),理由 。
(1)
(2)CD;
(3)NH4Fe(SO4)2·12H2O, 2NH4Fe(SO4)2+3Ba(OH)2==2Fe(OH)3↓+3BaSO4↓+ (NH4)2SO4。
(4)溶液由棕黄色变为浅绿色, 2Fe3+ + SO2 + 2H2O ====2Fe2+ + SO42- + 4H+。
(5)不合理,在配制溶液时,蒸馏水应加热煮沸,除去其中溶解的氧气。
【解析】
试题分析:根据题意知,该物质的摩尔质量为482g/mol,其中含有铁元素。由Ⅰ知,该物质含有Fe3+;由Ⅱ知,向含0.05mol溶质的溶液中加入足量的NaOH溶液,并加热,产生的气体经干燥后通入浓硫酸中,浓硫酸增重0.85g,则产生的氨气为0.05mol;产生的红褐色沉淀氢氧化铁经过过滤、洗涤、灼烧后得4.00g固体,其物质的量为0.025mol,则1mol该物质中含有1molNH4+和1molFe3+。由Ⅲ知,向含0.05mol溶质的溶液中加入足量的BaCl2溶液,产生不溶于盐酸的白色沉淀硫酸钡 23.30g,物质的量为0.1mol,则1mol该物质中含有2molSO42—;则结合该物质的摩尔质量判断,该物质的化学式为NH4Fe(SO4)2·12H2O。(1)实验Ⅱ中产生的气体为氨气,电子式为 。(2)该物质的化学式为NH4Fe(SO4)2·12H2O,其中含有NH4+和Fe3+,可用作含酚废水的检测试剂和肥料,选CD;(3)该物质的化学式为NH4Fe(SO4)2·12H2O,向该物质溶液中逐滴加入氢氧化钡溶液至铁元素完全沉淀时,生成硫酸钡、氢氧化铁和硫酸铵,化学反应方程式2NH4Fe(SO4)2+3Ba(OH)2==2Fe(OH)3↓+3BaSO4↓+ (NH4)2SO4。(4)将SO2气体通入该物质的溶液中,SO2与Fe3+发生氧化还原反应,Fe3+被还原为Fe2+,观察到的实验现象是溶液由棕黄色变为浅绿色,反应的离子方程式为2Fe3+ + SO2 + 2H2O ====2Fe2+ + SO42- + 4H+。(5)为了进一步验证该物质中铁元素的化合价,某同学设计了如下实验方案:取少量固体于试管中,加水充分溶解,滴加硫氰化钾溶液,若溶液显血红色,即可证明该物质中一定存在Fe3+。该实验操作不合理,理由在配制溶液时,蒸馏水应加热煮沸,除去其中溶解的氧气。
。(2)该物质的化学式为NH4Fe(SO4)2·12H2O,其中含有NH4+和Fe3+,可用作含酚废水的检测试剂和肥料,选CD;(3)该物质的化学式为NH4Fe(SO4)2·12H2O,向该物质溶液中逐滴加入氢氧化钡溶液至铁元素完全沉淀时,生成硫酸钡、氢氧化铁和硫酸铵,化学反应方程式2NH4Fe(SO4)2+3Ba(OH)2==2Fe(OH)3↓+3BaSO4↓+ (NH4)2SO4。(4)将SO2气体通入该物质的溶液中,SO2与Fe3+发生氧化还原反应,Fe3+被还原为Fe2+,观察到的实验现象是溶液由棕黄色变为浅绿色,反应的离子方程式为2Fe3+ + SO2 + 2H2O ====2Fe2+ + SO42- + 4H+。(5)为了进一步验证该物质中铁元素的化合价,某同学设计了如下实验方案:取少量固体于试管中,加水充分溶解,滴加硫氰化钾溶液,若溶液显血红色,即可证明该物质中一定存在Fe3+。该实验操作不合理,理由在配制溶液时,蒸馏水应加热煮沸,除去其中溶解的氧气。
考点:考查物质的组成测定及检验。


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源:2013-2014湖北省大冶市春季期末考试高二化学试卷(解析版) 题型:填空题
(9分)已知A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,J是一种黑色固体,I的浓溶液具有还原性,A~I均为中学化学常见物质,它们之间的转化关系如下图所示。(部分生成物和反应条件已略去)

请回答下列问题:
(1) 写出组成物质D的元素在周期表中的位置:___________________。
(2) ①写出反应①的化学方程式:______________________________。
②由E的饱和溶液可以制得胶体,用化学方程式表示该过程的原理是_________________________。
(3) 已知G的水溶液显碱性,其原因是(用离子方程式表示)_________。
(4) J在H2O2分解反应中作催化剂。若将适量J加入酸化的H2O2溶液中,J溶解生成它的+2价离子,该反应的离子方程式是___________________ 。
查看答案和解析>>
科目:高中化学 来源:2013-2014海口市第二学期高二化学期中考试(B卷)试卷(解析版) 题型:实验题
(12分)某兴趣小组同学进行乙醛的银镜反应,实验操作步骤如下:
A.在试管里先注入少量NaOH溶液,振荡,然后加热煮沸。把NaOH溶液倒去后,再用蒸馏水洗净试管备用。 B.在洗净的试管里配制银氨溶液。C.沿试管壁加入乙醛稀溶液。D.加热。请回答下列问题:
(1)步骤A中加NaOH溶液振荡,加热煮沸的目的是: 。
(2)步骤D应选择的加热方法是 (填下列装置编号)
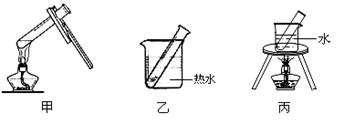
(3)乙醛发生银镜反应的化学方程式为: 。
(4)该兴趣小组的同学还对乙醛进行银镜反应的最佳实验条件进行了探究(部分实验数据如下表):

①实验1和实验2,探究的是 。
②当银氨溶液的量为1 mL,乙醛的量为3滴,温度为55℃,反应混合液pH为11时,出现银镜的时间为 min。(填范围)
③你认为探究乙醛进行银镜反应的最佳条件,除了测定银镜出现的时间外,还需要比较不同条件下形成的银镜的 。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省绍兴市柯桥区高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
(15分)太阳能电池是利用光电效应实现能量变化的一种新型装置,目前多采用单晶硅和多晶硅作为基础材料。高纯度的晶体硅可通过以下反应获得:
反应①(合成炉):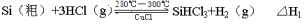
反应②(还原炉):
有关物质的沸点如下表所示:
物质 | BCl3 | PCl3 | SiCl4 | AsCl3 | AlCl3 | SiHCl3 |
沸点 | 12.1 | 73.5 | 57.0 | 129.4 | 180(升华) | 31.2 |
请回答以下问题:
(1)太阳能电池的能量转化方式为 ;由合成炉中得到的SiHCl3往往混有硼、磷、砷、铝等氯化物杂质,分离出SiHCl3的方法是 。
(2)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应①的KP= ;
(3)对于反应②,在0.1Mpa下,不同温度和氢气配比(H2/SiHCl3)对SiHCl3剩余量的影响如下表所示:

①该反应的△H2 0(填“>”、“<”、“=”)
②按氢气配比5:1投入还原炉中,反应至4min时测得HCl的浓度为0.12mol·L—1,则SiHCl3在这段时间内的反应速率为 。
③对上表的数据进行分析,在温度、配比对剩余量的影响中,还原炉中的反应温度选择在1100℃,而不选择775℃,其中的一个原因是在相同配比下,温度对SiHCl3 剩余量的影响,请分析另一原因是 。
(4)对于反应②,在1100℃下,不同压强和氢气配比(H2/SiHCl3)对SiHCl3剩余量的影响如图27—1所示:
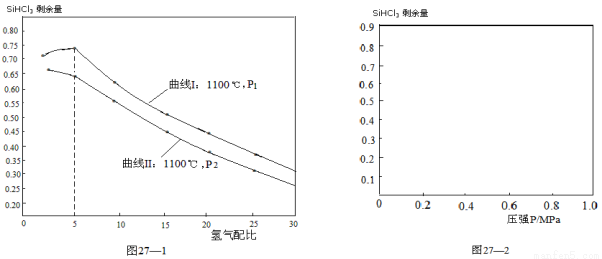
① 图中P1 P2(填“>”、“<”、“=”)
②在图27—2中画出氢气配比相同情况下,1200℃和1100℃的温度下,系统中SiHCl3剩余量随压强变化的两条变化趋势示意图。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省绍兴市柯桥区高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.常温下物质的量浓度相等的①(NH4)2CO3 ②(NH4)2SO4 ③ (NH4)2Fe(SO4)2三种溶液中水的电离程度:③>②>①
B.常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)

C.向Ca(OH)2溶液中加入过量的NaHCO3溶液:
Ca2++2HCO3-+2OH-→ CO32-+CaCO3↓+2H2O
D.25°C时,HCN溶液的电离平衡常数(Ka)与NaCN溶液的水解平衡常数(K)存在如下关系: Kw ·K = Ka
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省高三下学期联考理综化学试卷(解析版) 题型:选择题
五种短周期元素的某些信息如表所示:
元素 | 有关信息 |
X | 最高价氧化物对应的水化物能与其气态氢化物反应生成盐 |
Y | M层上有3个电子 |
Z | 短周期元素中原子半径最大的主族元素 |
W | 其单质是淡黄色固体 |
Q | 最高正价与最低负价代数和为6 |
下列说法正确的是
A.简单离子的半径大小顺序为:W>Q>Z>Y
B.Z单质在氧气中燃烧后的产物不能使品红溶液褪色
C.单质熔点高低的顺序为:Z>Y>X
D.Z与W元素只能形成原子个数比为2:1的化合物
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省湖州市高三二模理综化学试卷(解析版) 题型:选择题
由几种常见的盐混合组成的白色粉末,其中只可能含有Na+、K+、Al3+、CO32-、HCO3-、SO42-、NO2-中的若干种离子。某同学对该溶液进行如下实验:

以下说法正确的是
A.白色沉淀甲是Al(OH)3,气体甲是CO2,所以混合物一定含Al3+和HCO3-
B.气体乙一定是NO和NO2的混合气体
C.白色沉淀乙是BaSO4,所以原混合物一定含有SO42-
D.白色粉末中一定含有Na+ 、Al3+ 、NO2-
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省温州市业水平考试适应性测试化学试卷(解析版) 题型:选择题
下列事实中,能说明MOH是弱碱的有
①0.1mol/LMOH可以使酚酞试液变红
②0.1mol/LMCl溶液的呈酸性
③0.1mol/LMOH溶液的导电性比0.1mol/LNaOH溶液弱
④等体积的0.1mol/LMOH溶液与0.1mol/LHCl溶液恰好完全反应
A.①②③ B.②③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省高二下学期期中化学试卷(解析版) 题型:选择题
若CH2=CH2与Br2的加成反应的历程为:(1)Br2先变为Br+ 和Br-;(2)Br+ 先与CH2=CH2一端碳原子结合;(3)Br-与另一端碳原子结合。让CH2=CH2与Br2在含有NaCl和NaI的水溶液中反应,则得到的有机物不可能是 ( )
A.BrCH2CH2Br B.ClCH2CH2Cl C.BrCH2CH2I D.BrCH2CH2Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com